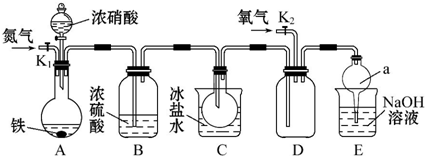
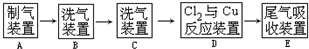
1.有人用全钒液流电池:VO2++V2++2H+$?_{充电}^{放电}$VO2++H2O+V3+,在空气中电解水(酸性条件下)的方法,阳极制得臭氧,阴极制得过氧化氢,电解总方程式为3H2O+3O2═3H2O2+O3,其中H2O2只为还原产物.下列说法正确的是( )
| A. | 原电池放电时正极反应为VO2++2H++e-═VO2++H2O | |
| B. | 充电时阴极反应为V2+-e-═V3+ | |
| C. | 电解池的阴极反应式为3O2+6H2O+6e-═3H2O2+6OH- | |
| D. | 电解池中生成22.4 L O3(标准状况)时,转移3 mol电子 |
18.甲、乙两种非金属元素,能说明甲比乙的非金属性强的是( )
①甲单质比乙单质容易与氢气化合
②甲元素的单质能与乙的阴离子发生氧化还原反应
③甲的最高价氧化物对应水化物的酸性比乙的最高价氧化物对应水化物的酸性强
④与某金属反应时,甲比乙得电子数多
⑤甲的单质熔沸点比乙的单质低.
①甲单质比乙单质容易与氢气化合
②甲元素的单质能与乙的阴离子发生氧化还原反应
③甲的最高价氧化物对应水化物的酸性比乙的最高价氧化物对应水化物的酸性强
④与某金属反应时,甲比乙得电子数多
⑤甲的单质熔沸点比乙的单质低.
| A. | 只有③④ | B. | 只有①②⑤ | C. | 只有①②③ | D. | ①②③④⑤ |
17.常温下,某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为5:2,用石墨作电极电解该混合溶液时,根据电解产物,可分为三个阶段,下列叙述不正确的是( )
| A. | 溶液pH不断增大,最后为7 | B. | 阳极先析出Cl2,后析出O2 | ||
| C. | 阴极始终只析出H2 | D. | 电解最后阶段为电解水 |
16.在下列有机物分子中,核磁共振氢谱中给出的信号峰数目相同的一组是( )


| A. | ①⑤ | B. | ②④ | C. | ④⑤ | D. | ⑤⑥ |
15.下列叙述或实验方案不合理的是( )
0 156433 156441 156447 156451 156457 156459 156463 156469 156471 156477 156483 156487 156489 156493 156499 156501 156507 156511 156513 156517 156519 156523 156525 156527 156528 156529 156531 156532 156533 156535 156537 156541 156543 156547 156549 156553 156559 156561 156567 156571 156573 156577 156583 156589 156591 156597 156601 156603 156609 156613 156619 156627 203614
| A. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极产生的Cl2进入阳极室 | |
| B. | 用水可以一次性鉴别硝基苯、甲苯、冰醋酸三种物质 | |
| C. | 制硫酸和氢氧化钠:用如图所示装置 (注:b为阴离子交换膜、c为阳离子交换膜) (注:b为阴离子交换膜、c为阳离子交换膜) | |
| D. | 乙醛的氧化:在试管里加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液4滴~6滴,振荡后加入乙醛溶液0.5 mL,加热至沸腾 |
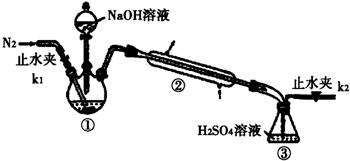
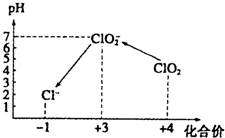 ClO2气体是一种在水处理等方面有广泛应用的高效安全消毒剂.我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
ClO2气体是一种在水处理等方面有广泛应用的高效安全消毒剂.我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.