3.Ⅰ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
(1)从甲组情况分析,(填“能”或“不能”)不能判断HA是强酸还是弱酸.
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)相等,则乙组混合溶液中存在3个动态平衡.
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+)
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=10-4-10-10mol•L-1
(5)用离子方程式解释丁溶液pH=10的原因是A-+H2O?HA+OH-.
Ⅱ.某二元酸(化学式用H2B表示)水溶液电离是:H2B=H++HB- HB-?H++B2-.
回答下列问题:
(6)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是A.
A.c( B2-)+c(HB-)=0.1mol/L
B.c(Na+)=2( c( B2-)+c(HB-)+c(H2B))
C.c(OH-)=c(H+)+c(HB-)+2c(H2B)
D.c(Na+)+c(H+)=c(OH-)+c(HB-)+c( B2-)
| 实验编号 | HA的物质的量浓度(mol•L-1) | NaOH的物质的量浓度(mol•L-1) | 混合后溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)相等,则乙组混合溶液中存在3个动态平衡.
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+)
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=10-4-10-10mol•L-1
(5)用离子方程式解释丁溶液pH=10的原因是A-+H2O?HA+OH-.
Ⅱ.某二元酸(化学式用H2B表示)水溶液电离是:H2B=H++HB- HB-?H++B2-.
回答下列问题:
(6)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是A.
A.c( B2-)+c(HB-)=0.1mol/L
B.c(Na+)=2( c( B2-)+c(HB-)+c(H2B))
C.c(OH-)=c(H+)+c(HB-)+2c(H2B)
D.c(Na+)+c(H+)=c(OH-)+c(HB-)+c( B2-)
2.25℃时,由水电离出c(OH-)=1×10-11mol/L 的溶液中,一定能大量共存的离子组是( )
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、CH3COO-、K+、CO32- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | K+、NO3-、Cl-、Na+ |
1.有主族元素A、B、C、D、E,相对位置如图所示.C的原子序数是D的两倍.
(1)E位于元素周期表中第四周期,第VA族,该周期共有18种元素
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是(写酸的化学式)H2SO4
(3)上述五种元素的氢化物稳定性最强的是(写氢化物的化学式)H2O,用电子式表示该物质的形成过程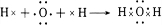 .
.
| D | ||
| A | B | C |
| E |
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是(写酸的化学式)H2SO4
(3)上述五种元素的氢化物稳定性最强的是(写氢化物的化学式)H2O,用电子式表示该物质的形成过程
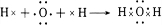 .
.
19. 请根据下表,回答下列问题:(数据均在25℃时测定)
请根据下表,回答下列问题:(数据均在25℃时测定)
(1)物质的量浓度为0.1mol•L-1的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,由水电离产生的H+由大到小的顺序是a>b>d>c(填编号).
(2)常温下0.1mol•L-1的HClO溶液加水稀释过程,下列表达式的数据不变的是D;
A.c (H+) B.$\frac{c({H}^{+})}{c(HClO)}$C.$\frac{c(O{H}^{-})}{c({H}^{+})}$D.$\frac{c(Cl{O}^{-})}{c(HClO)•c(O{H}^{-})}$
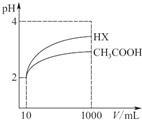
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图所示,则Ka(HX)> (选填>、=、<,下同) Ka(CH3COOH);若将浓度为c1的NaOH溶液与0.1mol/L的HX等体积混合,
所得溶液的pH=7,则c1<0.1mol/L,溶液中离子浓度的大小关系为:c(Na+)=c(X-)>c(OH-)=c(H+);若将“0.1mol/L的HX”改为“pH=1的HX”,所得溶液的pH仍为7,则c1>0.1mol/L.
(4)室温下,如果将0.1mol CH3COONa和0.05mol HCl溶于水,形成混合溶液(体积不变)
①CH3COOH和CH3COO-两种粒子的物质的量之和等于0.1mol.
②CH3COO-和OH-两种粒子的物质的量之和比H+多0.05mol.
(5)某硫酸铜溶液里c(Cu2+)=0.02mol•L-1,如要生成Cu(OH)2,应调整溶液pH,使之大于5;要使0.2mol•L-1硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液,使溶液pH为6.
 请根据下表,回答下列问题:(数据均在25℃时测定)
请根据下表,回答下列问题:(数据均在25℃时测定)| 化学式 | CH3COOH | H2CO3 | HClO | Cu(OH)2 |
| 相关常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 | Ksp=2×10-20 |
(2)常温下0.1mol•L-1的HClO溶液加水稀释过程,下列表达式的数据不变的是D;
A.c (H+) B.$\frac{c({H}^{+})}{c(HClO)}$C.$\frac{c(O{H}^{-})}{c({H}^{+})}$D.$\frac{c(Cl{O}^{-})}{c(HClO)•c(O{H}^{-})}$
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图所示,则Ka(HX)> (选填>、=、<,下同) Ka(CH3COOH);若将浓度为c1的NaOH溶液与0.1mol/L的HX等体积混合,
所得溶液的pH=7,则c1<0.1mol/L,溶液中离子浓度的大小关系为:c(Na+)=c(X-)>c(OH-)=c(H+);若将“0.1mol/L的HX”改为“pH=1的HX”,所得溶液的pH仍为7,则c1>0.1mol/L.
(4)室温下,如果将0.1mol CH3COONa和0.05mol HCl溶于水,形成混合溶液(体积不变)
①CH3COOH和CH3COO-两种粒子的物质的量之和等于0.1mol.
②CH3COO-和OH-两种粒子的物质的量之和比H+多0.05mol.
(5)某硫酸铜溶液里c(Cu2+)=0.02mol•L-1,如要生成Cu(OH)2,应调整溶液pH,使之大于5;要使0.2mol•L-1硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液,使溶液pH为6.
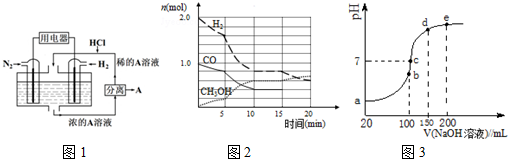
18.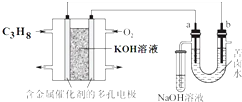 用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
 用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )| A. | 电池工作时,负极反应式为:C3H8+26OH--20e-═3CO${\;}_{3}^{2-}$+17H2O | |
| B. | 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 | |
| C. | 电解时,电子流动的路径是:负极→外电路→阴极→溶液→阳极→正极 | |
| D. | 忽略能量损耗,当电池中消耗 0.16 g O2时,a极周围会产生0.71 g Cl2 |
17.下列关于pH值的叙述正确的是( )
| A. | 常温下,4体积pH=9的Ca(OH)2溶液与1体积pH=13的NaOH溶液混合后,氢离子浓度是1×10-13mol/L | |
| B. | 用盐酸滴定氨水时,能用酚酞做指示剂(酚酞的变色范围是pH=8~10) | |
| C. | 加热Na2CO3溶液、NaHCO3溶液和CO2与H2O饱和溶液,它们的pH值都会上升 | |
| D. | pH相同的氨水、氢氧化钠用蒸馏水稀释到原来的x倍、y倍至pH仍相同,则x<y |
16.现有两种气态烃的混合气体,通过不同实验分别测出下列数据
①1mol该混合烃,在空气中燃烧得到1.5molCO2;
②125℃时,1L某气态烃在9L氧气中充分燃烧反应后的混合气体体积仍为10L(相同条件下);
③0.3moL混和烃完全燃烧生成10.8gH2O;
④相同条件下,该混合烃的密度是氢气的 10倍;
⑤实验测出混合气体中碳原子和氢原子的比值为1:3
⑥60g混合烃完全燃烧生成108gH2O.
上述数据可以直接说明混合烃中一定存在甲烷的是( )
0 156431 156439 156445 156449 156455 156457 156461 156467 156469 156475 156481 156485 156487 156491 156497 156499 156505 156509 156511 156515 156517 156521 156523 156525 156526 156527 156529 156530 156531 156533 156535 156539 156541 156545 156547 156551 156557 156559 156565 156569 156571 156575 156581 156587 156589 156595 156599 156601 156607 156611 156617 156625 203614
①1mol该混合烃,在空气中燃烧得到1.5molCO2;
②125℃时,1L某气态烃在9L氧气中充分燃烧反应后的混合气体体积仍为10L(相同条件下);
③0.3moL混和烃完全燃烧生成10.8gH2O;
④相同条件下,该混合烃的密度是氢气的 10倍;
⑤实验测出混合气体中碳原子和氢原子的比值为1:3
⑥60g混合烃完全燃烧生成108gH2O.
上述数据可以直接说明混合烃中一定存在甲烷的是( )
| A. | ①②③④⑤⑥ | B. | ①②③⑥ | C. | ③④⑤⑥ | D. | ①④⑤⑥ |
 .
.
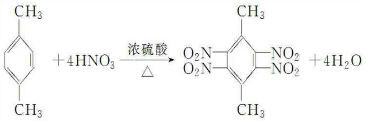 .
.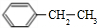 、
、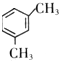 .
.