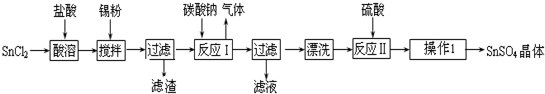
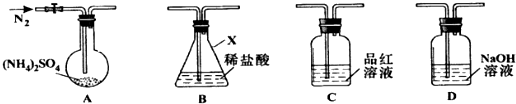
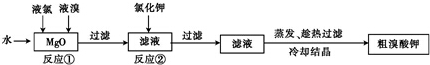
5.下列说法正确的是( )
| A. | 化合反应均是放热反应 | B. | 中和反应都是放热反应 | ||
| C. | 吸热反应只吸收外界能量 | D. | 氧化还原反应均是放热反应 |
4.关于甲烷和乙烯,说法正确的是( )
| A. | 甲烷能燃烧,乙烯不能 | |
| B. | 甲烷和乙烯都能使溴水褪色 | |
| C. | 甲烷和乙烯都能使酸性高锰酸钾溶液褪色 | |
| D. | 甲烷和乙烯完全燃烧的产物都是CO2和H2O |
3.将下列物质加入鸡蛋清中,出现白色沉淀,加水沉淀不会溶解的是( )
| A. | NH4Cl | B. | NaCl | C. | KCl | D. | BaCl2 |
2.决定化学反应速率的主要因素是( )
| A. | 温度 | B. | 反应物的性质 | C. | 浓度 | D. | 催化剂 |
20.下列各组混合物,可以用分液漏斗分离的是( )
| A. | 水和酒精 | B. | 四氯化碳和水 | C. | 溴和溴苯 | D. | 汽油和煤油 |
17.Ⅰ.Fe3+具有氧化性,实验室测定含碘废液中I-的含量的过程如下:量取25.00mL废液于250mL锥形瓶中,分别加入5mL 2mol•L-1 H2SO4和10mL 20% Fe2(SO4)3溶液,摇匀.小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入几滴二苯胺磺酸钠(用作指示剂),用0.02500mol•L-1标准K2Cr2O7溶液进行滴定到终点.重复3次,数据记录如表:
(1)在盛有废液的锥形瓶中先加入5mL 2mol•L-1 H2SO4的目的是Fe3++3H2O?Fe(OH)3+3H+,加入H2SO4平衡逆向移动,抑制Fe3+水解.(用离子方程式和语言叙述解释)
(2)上述过程中涉及的反应:①2Fe3++2I-═2Fe2++I2②6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O.
(3)根据滴定有关数据,该废液中I-含量是15.24g•L-1.
(4)在滴定过程中,下列操作(其他操作正确)会造成测定结果偏低的是A.
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗衣后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡.
Ⅱ.Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点.某学习小组同学设计如下实验:
请回答:
(1)设计实验①的目的是排除NO3-的干扰.
(2)实验③可得出结论是Fe3+能氧化Ag.
(3)写出实验②中反应的离子方程式Fe2++Ag+?Fe3++Ag.
(4)根据以上实验,Fe3+和Ag+的氧化性相对强弱与离子浓度有关.
0 156420 156428 156434 156438 156444 156446 156450 156456 156458 156464 156470 156474 156476 156480 156486 156488 156494 156498 156500 156504 156506 156510 156512 156514 156515 156516 156518 156519 156520 156522 156524 156528 156530 156534 156536 156540 156546 156548 156554 156558 156560 156564 156570 156576 156578 156584 156588 156590 156596 156600 156606 156614 203614
| 次数 | 1 | 2 | 3 |
| 滴定体积/mL | 19.98 | 20.02 | 19.00 |
(2)上述过程中涉及的反应:①2Fe3++2I-═2Fe2++I2②6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O.
(3)根据滴定有关数据,该废液中I-含量是15.24g•L-1.
(4)在滴定过程中,下列操作(其他操作正确)会造成测定结果偏低的是A.
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗衣后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡.
Ⅱ.Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点.某学习小组同学设计如下实验:
| 实验编号 | 实验操作 | 现象 |
| 1 | 向10mL 3mol/L KNO3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 无白色沉淀生成 |
| 2 | 向10mL 1mol/L AgNO3溶液中滴加2mL 0.1mol/L FeSO4溶液,振荡,再滴加酸性KMnO4溶液 | 紫红色不褪去 |
| 3 | 向10mL 1mol/L Fe(NO3)3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 有白色沉淀生成 |
(1)设计实验①的目的是排除NO3-的干扰.
(2)实验③可得出结论是Fe3+能氧化Ag.
(3)写出实验②中反应的离子方程式Fe2++Ag+?Fe3++Ag.
(4)根据以上实验,Fe3+和Ag+的氧化性相对强弱与离子浓度有关.