5.汽车尾气中的CO、NO都是城市空气中浓度较高、危害严重的污染物,下列有关它们的叙述中不正确的是( )
| A. | CO、NO均难溶于水 | |
| B. | CO、NO均为酸性氧化物 | |
| C. | CO、NO均为无色无味的有毒气体 | |
| D. | 在催化剂的作用下,可通过反应2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2来达到净化汽车尾气的目的 |
4.下列说法中不 正确的是( )
| A. | 1 mol CH≡CH可以与Br2发生加成反应,消耗2 mol Br2 | |
| B. | 苯的邻位二元取代物只有一种可以说明苯分子不具有碳碳单键和碳碳双键的交替结构 | |
| C. | 2甲基戊烷的沸点高于己烷 | |
| D. | 用水可区分苯和溴苯 |
3.若把周期表原先的主、副族号取消,由左到右按原顺序编为18纵行.如碱金属为第1纵行,稀有气体为第18纵行,按这个规定,下列说法不正确的是( )
| A. | 计算机芯片的组成元素位于第14纵行 | |
| B. | 第10纵行元素全部是金属元素 | |
| C. | 第3纵行元素的种类最多 | |
| D. | 只有第2纵行元素的原子最外层有2个电子 |
18. 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
(1)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+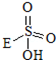 →
→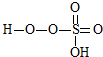 +HE (请写出横线上物质的结构式)
+HE (请写出横线上物质的结构式)
(4)F位于d区,价电子排布式为3d54s1.
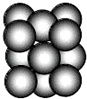
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}π}{6}$.
 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F 是前四周期原子电子轨道表示式中单电子数最多的元素 |
| G在周期表的第十一列 |
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+
 →
→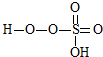 +HE (请写出横线上物质的结构式)
+HE (请写出横线上物质的结构式)(4)F位于d区,价电子排布式为3d54s1.
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}π}{6}$.
16.下列各项比较中前者高于(或大于或强于)后者的是( )
0 156414 156422 156428 156432 156438 156440 156444 156450 156452 156458 156464 156468 156470 156474 156480 156482 156488 156492 156494 156498 156500 156504 156506 156508 156509 156510 156512 156513 156514 156516 156518 156522 156524 156528 156530 156534 156540 156542 156548 156552 156554 156558 156564 156570 156572 156578 156582 156584 156590 156594 156600 156608 203614
| A. | CCl4和SiCl4的熔点 | B. | NH3与H2O的键角 | ||
| C. | SO2和CO2在水中的溶解度 | D. | 碳化硅和金刚石的硬度 |
 有机物M的结构简式如图所示.
有机物M的结构简式如图所示. 人们对苯及芳香烃的认识有一个不断深化的过程.
人们对苯及芳香烃的认识有一个不断深化的过程. :该结构的一氯代物有1种.
:该结构的一氯代物有1种. ,下列关于萘的说法正确的是CD(填编号)
,下列关于萘的说法正确的是CD(填编号)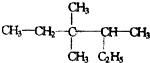 3,3,4-三甲基己烷
3,3,4-三甲基己烷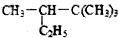 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷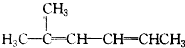 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯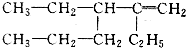 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.
 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B- 少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+ 与D2- 离子数之比为2:1.请回答下列问题:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B- 少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+ 与D2- 离子数之比为2:1.请回答下列问题: ,在CB3 分子中C元素原子的原子轨道发生的是sp3 杂化.
,在CB3 分子中C元素原子的原子轨道发生的是sp3 杂化.