15.已知下列热化学方程式:
①Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H1
②Hg(l)+$\frac{1}{2}$O2(g)═HgO(s)△H2,
则反应Zn(s)+HgO(s)═ZnO(s)+Hg(l)△H3中△H3的值为( )
①Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H1
②Hg(l)+$\frac{1}{2}$O2(g)═HgO(s)△H2,
则反应Zn(s)+HgO(s)═ZnO(s)+Hg(l)△H3中△H3的值为( )
| A. | △H1-△H2 | B. | △H2-△H1 | C. | △H1+△H2 | D. | -(△H1-△H2) |
14.下列反应的离子方程式不正确的是( )
| A. | 侯氏制碱法的基本原理:Na++NH3+H2O+CO2=NaHCO3↓+NH4+ | |
| B. | 向KAl(SO4)2溶液中加入Ba(OH)2溶液至中性:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 硫酸亚铁溶液中滴加酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O | |
| D. | 向漂白粉溶液中通入少量的SO2气体:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
13.下列推断合理的是( )
| A. | 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 | |
| B. | 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 | |
| C. | 常温下Fe、Al遇浓HNO3发生钝化,故Fe、Al不能与浓HNO3发生反应 | |
| D. | 将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
11.选用适当的试剂和方法除去下列物质中的杂质(括号内)填表:
| 混合物 | 除杂质的试剂 | 除杂质的方法 |
| 苯(苯酚) | NaOH溶液 | 分液 |
| 酒精(水) | 生石灰 | 蒸馏 |
| 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
8. 某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积的变化),实验结果如图所示,下列说法错误的是( )
某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积的变化),实验结果如图所示,下列说法错误的是( )
 某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积的变化),实验结果如图所示,下列说法错误的是( )
某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积的变化),实验结果如图所示,下列说法错误的是( )| A. | AB段反应速率最快的原因可能是反应放热,体系温度升高 | |
| B. | BC段反应速率变慢的原因可能是盐酸浓度降低 | |
| C. | 该反应速率也可以用CaCl2的浓度变化与时间关系来表示 | |
| D. | C点后CO2体积不变的原因一定是大理石消耗完 |
7.将0.1mol/L的NaHC2O4溶液与0.1mol/L的NaOH溶液等体积混合后,关于该混合溶液说法不正确的是( )
| A. | 该混合溶液中有:c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+2 c(C2O42-) | |
| B. | 该混合溶液中有:c( Na+)=2[c(HC2O4-)+c(H2C2O4)+c(C2O42-)] | |
| C. | 该混合溶液中有:c(OH-)-c(H+)=c(HC2O4-)+2 c(H2C2O4) | |
| D. | 该混合溶液中有:c(Na+)>c(C2O42-)>c(HC2O4-)>c(OH-)>c(H+) |
6.下列粒子半径之比大于1的是( )
0 156411 156419 156425 156429 156435 156437 156441 156447 156449 156455 156461 156465 156467 156471 156477 156479 156485 156489 156491 156495 156497 156501 156503 156505 156506 156507 156509 156510 156511 156513 156515 156519 156521 156525 156527 156531 156537 156539 156545 156549 156551 156555 156561 156567 156569 156575 156579 156581 156587 156591 156597 156605 203614
| A. | r(Al)/r(Na) | B. | r(C)/r(Si) | C. | r(F?)/r(Mg2+) | D. | r(Fe2+)/r(Fe) |
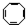 互为同分异构体且属于芳香烃的有机物的结构简式
互为同分异构体且属于芳香烃的有机物的结构简式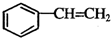 .
. 、
、 .
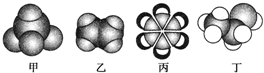
.
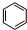 ,丁CH3CH2OH
,丁CH3CH2OH +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$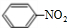 +H2O
+H2O