15.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A. | X与Y形成化合物时,X可以显负价,Y显正价 | |
| B. | 在元素同周期表中X可能位于Y的右面 | |
| C. | 最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 | |
| D. | Y的气态氢化物的稳定性小于X的气态氢化物的稳定性 |
14.科学家将水置于一个足够强的电场中,在20℃时水分子瞬间凝固形成“暖冰”.下列关于“暖冰”的说法正确的是( )
| A. | 暖冰中水分子是一种非常稳定的化合物,这是由于氢键所致 | |
| B. | 暖冰中水分子的各原子均满足8电子稳定结构 | |
| C. | 水凝固形成20℃时的“暖冰”所发生的变化是化学变化 | |
| D. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
13.下列说法正确的是( )
| A. | 电子在1s轨道上运动像地球围绕太阳旋转 | |
| B. | 2s的电子云半径比1s电子云半径大,说明2s能级的电子比1s的多 | |
| C. | 1s轨道的电子云形状为圆形的面 | |
| D. | nf能级中最多可容纳14个电子 |
12.关于反应:
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJmol-1
下列叙述正确的是( )
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJmol-1
下列叙述正确的是( )
| A. | CO的燃烧热为-283 kJ/mol | |
| B. | 在③反应时,若加入催化剂,可以使△H减小 | |
| C. | 若投入1molCO2和3molH2在一定条件下充分反应,则放出热量49 kJ | |
| D. | 若生成相同质量的CO2,则放出的热量C2H2大于CO |
11.下列事实中,不能用勒夏特列原理解释的是( )
| A. | 溴水中有下列平衡:Br2+H2O?HBr+HBrO当加入AgNO3(s)后溶液颜色变浅 | |
| B. | 2NO2(g)?N2O4(g)△H<0,升高温度可使体系颜色加深 | |
| C. | 反应N2+3H2?2NH3△H<0,增大压强可提高N2的转化率 | |
| D. | 合成氨反应CO+NO2?CO2+NO△H>0中使用催化剂 |
10.在2A+B?3C+4D中,表示该反应速率最快的是( )
| A. | υ(A)=0.5mol•L-1•S-1 | B. | υ(B)=0.3 mol•L-1•S-1 | ||
| C. | υ(C)=0.8mol•L-1•S-1 | D. | υ(D)=6 mol•L-1•min-1 |
7.某元素的一种同位素X的原子质量数为A,含N个中子,它与${\;}_{1}^{2}$H原子组成HmX分子,在agHmX中所含质子的物质的量是( )
0 156409 156417 156423 156427 156433 156435 156439 156445 156447 156453 156459 156463 156465 156469 156475 156477 156483 156487 156489 156493 156495 156499 156501 156503 156504 156505 156507 156508 156509 156511 156513 156517 156519 156523 156525 156529 156535 156537 156543 156547 156549 156553 156559 156565 156567 156573 156577 156579 156585 156589 156595 156603 203614
| A. | $\frac{a}{A}$(A-N+2m)mol | B. | $\frac{a}{A+m}$(A-N)mol | C. | $\frac{a}{A+m}$(A-N+2m)mol | D. | $\frac{a}{A+2m}$(A-N+m)mol |
 .
. .
.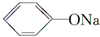 +CH3I→
+CH3I→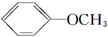 +NaI
+NaI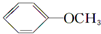 +HI→
+HI→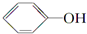 +CH3l
+CH3l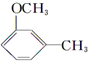 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$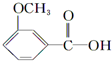
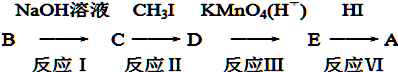
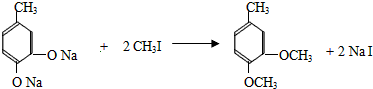 .
. .
.