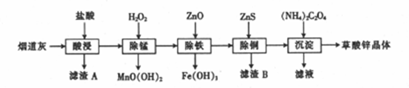
8.以炼锌厂的烟道灰如图(主要成分为ZnO,还含有少量Fe2O3、CuO、SiO2、MnO等)为原料可生产草酸锌晶体(ZnC2O4•2H2O).
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
已知:Ksp(FeS)=1.4×10-39,Ksp(MnS)=1.4×10-13.
(1)滤渣A的主要成分为SiO2(填化学式).
(2)生成滤渣B的离子方程式为ZnS+Cu2+=CuS+Zn2+.
(3)除铁时加入ZnO控制反应液的pH范围为3.3~5.4.
(4)该炼锌厂废气中含有H2S,可用FeCl3溶液吸收H2S,得到单质硫,过滤后,再以石墨为电极,在一定条件下电解滤液.
①FeCl3与H2S反应的离子方程式为2Fe3++H2S=2Fe2++S↓+2H+.
②电解池中阴极的电极反应式为2H+-2e-=H2↑.
(5)25℃时,向0.10mol•L-1的H2S溶液中通入HCl气体或加入NaOH固体以调节溶液pH与c(S2-)的关系如图2所示(忽略溶液体积的变化和H2S的挥发)
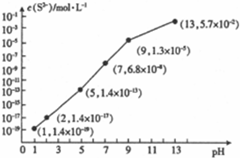
①pH=13时,溶液中的c(H2S)+c(HS-)=0.043mol•L-1
②某溶液中含未知浓度的Mn2+、0.01mol•L-1Fe2+和0.10mol•L-1H2S,当溶液pH=2时,Fe2+ 开始沉淀,当Mn2+开始沉淀时,溶液中
$\frac{c(M{n}^{2+})}{c(F{e}^{2+})}$=2×106.

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 1.9 | 6.5 | 4.2 | 5.4 |
| 完全沉淀时的pH | 3.3 | 9.7 | 6.7 | 8.2 |
(1)滤渣A的主要成分为SiO2(填化学式).
(2)生成滤渣B的离子方程式为ZnS+Cu2+=CuS+Zn2+.
(3)除铁时加入ZnO控制反应液的pH范围为3.3~5.4.
(4)该炼锌厂废气中含有H2S,可用FeCl3溶液吸收H2S,得到单质硫,过滤后,再以石墨为电极,在一定条件下电解滤液.
①FeCl3与H2S反应的离子方程式为2Fe3++H2S=2Fe2++S↓+2H+.
②电解池中阴极的电极反应式为2H+-2e-=H2↑.
(5)25℃时,向0.10mol•L-1的H2S溶液中通入HCl气体或加入NaOH固体以调节溶液pH与c(S2-)的关系如图2所示(忽略溶液体积的变化和H2S的挥发)

①pH=13时,溶液中的c(H2S)+c(HS-)=0.043mol•L-1
②某溶液中含未知浓度的Mn2+、0.01mol•L-1Fe2+和0.10mol•L-1H2S,当溶液pH=2时,Fe2+ 开始沉淀,当Mn2+开始沉淀时,溶液中
$\frac{c(M{n}^{2+})}{c(F{e}^{2+})}$=2×106.
7.工业利用NaOH溶液或氨水喷淋捕捉空气中的CO2制造甲醇,流程图如图1所示:
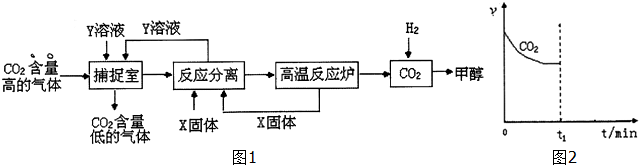
(1)下列有关捕捉空气中的CO2过程中的叙述不正确的有BD.
A、X选用CaO,而且要循环利用CaO与Y溶液
B、捕捉室里温度越高越有利于CO2 的捕捉
C、开放高效光催化剂分解水制氢气,是降低合成甲醇成本的有效途径
D、该捕捉CO2技术的应用有利于缓解全球变暖,而且能耗小
(2)在捕捉室用稀氨水喷淋“捕捉”空气中的CO2时,有NH2COONH4(氨基甲酸胺)生成.现将一定量纯净的氨基甲酸胺置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应
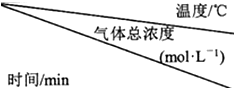
NH2COONH4(s)?2NH3(g)+CO2(g)达到分解平衡.实验测得不同温度及反应时间(t1<t2<t3)的有关表:氨基甲酸铵分解时温度、气体总浓度及反应时间的关系
①氨基甲酸胺分解反应为吸热反应(选填“吸热”、“放热”).在25℃,0-t1时间内产生氨气的平均速率为:$\frac{1.8}{{t}_{1}}$×10-3mol/(L.min).
②根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)?NH2COONH4(s)平衡常数K约为4.9×108.
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H<0.
①将1mol CO2和3mol H2充入恒温恒压的密闭容器中发生上述反应,CO2消耗速率v(CO2)与时间关系如图2所示.若在时间t1时,向容器中再充入1mol CO2和3mol H2,请在图中画出CH3OH生成速率v(CH3OH)与时间的关系曲线.
②在一个恒温固定容积的密闭容器中,加入1mol CO2和3mol H2,充分反应后达到平衡放出热量为aKJ.若在原来的容器中加入2mol CO2和6mol H2,在相同温度下充分反应,达到平衡放出热量为bKJ.则a和b满足的关系b>2a.

(1)下列有关捕捉空气中的CO2过程中的叙述不正确的有BD.
A、X选用CaO,而且要循环利用CaO与Y溶液
B、捕捉室里温度越高越有利于CO2 的捕捉
C、开放高效光催化剂分解水制氢气,是降低合成甲醇成本的有效途径
D、该捕捉CO2技术的应用有利于缓解全球变暖,而且能耗小
(2)在捕捉室用稀氨水喷淋“捕捉”空气中的CO2时,有NH2COONH4(氨基甲酸胺)生成.现将一定量纯净的氨基甲酸胺置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应
NH2COONH4(s)?2NH3(g)+CO2(g)达到分解平衡.实验测得不同温度及反应时间(t1<t2<t3)的有关表:氨基甲酸铵分解时温度、气体总浓度及反应时间的关系
 | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 0.9×10-3 | 2.7×10-3 | 8.1×10-3 |
| t2 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
| t3 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
②根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)?NH2COONH4(s)平衡常数K约为4.9×108.
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H<0.
①将1mol CO2和3mol H2充入恒温恒压的密闭容器中发生上述反应,CO2消耗速率v(CO2)与时间关系如图2所示.若在时间t1时,向容器中再充入1mol CO2和3mol H2,请在图中画出CH3OH生成速率v(CH3OH)与时间的关系曲线.
②在一个恒温固定容积的密闭容器中,加入1mol CO2和3mol H2,充分反应后达到平衡放出热量为aKJ.若在原来的容器中加入2mol CO2和6mol H2,在相同温度下充分反应,达到平衡放出热量为bKJ.则a和b满足的关系b>2a.
2.用中和滴定法测定烧碱的纯度(烧碱中的杂质不和酸反应),请根据实验回答:
(1)将称量好的4.3g烧碱样品配制成250mL待测液,配制过程使用的主要仪器除250mL容量瓶、量筒、烧杯、胶头滴管外,还有一种必须使用的仪器是玻璃棒.
(2)用碱式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞.
(3)用0.20mol•L-1的标准盐酸滴定待测液,判断滴定终点的现象是:滴入最后一滴盐酸时,锥形瓶内溶液恰好由红色变无色,并且半分钟内不变色.
(4)如果实验操作正确,从滴定开始到结束,溶液中的离子浓度关系可以出现的是B、C(填答案字母序号)
A.c(Na+)>c(Cl-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(Cl-)>c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(Cl-)
D.c(Na+)+c(H+)>c(OH-)+c(Cl-)
(5)根据下列数据计算,c(NaOH)=0.40mol/L,烧碱的纯度为93%(保留整数)
(6)经过分析发现,本次实验的测定结果比烧碱的实际纯度偏高,造成误差的可能原因是C、D(填答案字母序号)
A.滴定前平视,滴定后俯视 B.用标准液润洗滴定管
C.用待测液润洗锥形瓶 D.不小心将标准液滴在锥形瓶外面
E.滴定接近终点时,用少量蒸馏水冲洗锥形瓶内.
(1)将称量好的4.3g烧碱样品配制成250mL待测液,配制过程使用的主要仪器除250mL容量瓶、量筒、烧杯、胶头滴管外,还有一种必须使用的仪器是玻璃棒.
(2)用碱式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞.
(3)用0.20mol•L-1的标准盐酸滴定待测液,判断滴定终点的现象是:滴入最后一滴盐酸时,锥形瓶内溶液恰好由红色变无色,并且半分钟内不变色.
(4)如果实验操作正确,从滴定开始到结束,溶液中的离子浓度关系可以出现的是B、C(填答案字母序号)
A.c(Na+)>c(Cl-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(Cl-)>c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(Cl-)
D.c(Na+)+c(H+)>c(OH-)+c(Cl-)
(5)根据下列数据计算,c(NaOH)=0.40mol/L,烧碱的纯度为93%(保留整数)
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
A.滴定前平视,滴定后俯视 B.用标准液润洗滴定管
C.用待测液润洗锥形瓶 D.不小心将标准液滴在锥形瓶外面
E.滴定接近终点时,用少量蒸馏水冲洗锥形瓶内.
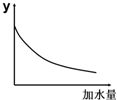
1.25℃时,0.1mol/L稀醋酸加水稀释,如图坐标中的纵坐标y可以是( )
0 156389 156397 156403 156407 156413 156415 156419 156425 156427 156433 156439 156443 156445 156449 156455 156457 156463 156467 156469 156473 156475 156479 156481 156483 156484 156485 156487 156488 156489 156491 156493 156497 156499 156503 156505 156509 156515 156517 156523 156527 156529 156533 156539 156545 156547 156553 156557 156559 156565 156569 156575 156583 203614

| A. | 溶液的pH | B. | 溶液的导电能力 | ||
| C. | 醋酸的电离平衡常数 | D. | 醋酸的c (OH-) |
 H2PO4-+H+.
H2PO4-+H+.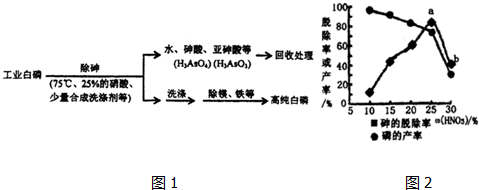

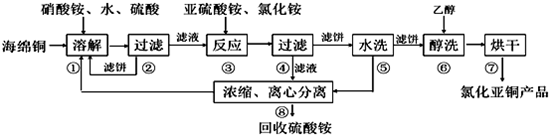
 如图所示实验装置可用于制取乙炔.
如图所示实验装置可用于制取乙炔.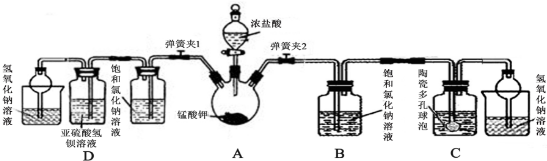
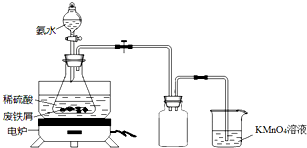 某实验小组用废铁屑(含少量S等元素)为原料制备三草酸合铁(Ⅲ)酸钾晶体[K3Fe(C2O4)3•3H2O]并测定其组成.
某实验小组用废铁屑(含少量S等元素)为原料制备三草酸合铁(Ⅲ)酸钾晶体[K3Fe(C2O4)3•3H2O]并测定其组成.