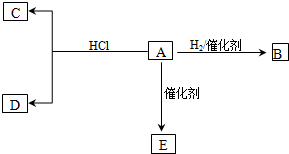
18.W、X、Y、Z、M、Q均为除稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的4倍,Z与M的最低负化合价相同,X、M在周期表中位置如图所示.
(1)Y在周期表中的位置为第二周期第IVA族,Q的元素名称为氯;
(2)X元素的最高价氧化物的电子式为 ;
;
(3)元素的非金属性:M<Q(填“>”、“<”或“=”),写出一个证明此结论的化学方程式H2S+Cl2=2S↓+2HCl;
(4)Z与W形成的4核10个电子离子的电子式为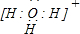 ;
;
(5)X、Y可分别与Z以原子个数比1:1形成化合物丙和丁.在催化剂存在条件下,丙与丁发生反应,生成单质Y2和另一种化合物戊.写出该反应的化学方程式:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
| X | ||
| M |
(2)X元素的最高价氧化物的电子式为
 ;
;(3)元素的非金属性:M<Q(填“>”、“<”或“=”),写出一个证明此结论的化学方程式H2S+Cl2=2S↓+2HCl;
(4)Z与W形成的4核10个电子离子的电子式为
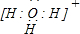 ;
;(5)X、Y可分别与Z以原子个数比1:1形成化合物丙和丁.在催化剂存在条件下,丙与丁发生反应,生成单质Y2和另一种化合物戊.写出该反应的化学方程式:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
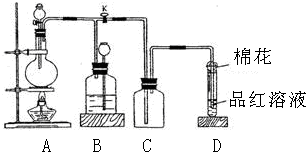
17.有机物M可从酸牛奶中提取.已知纯净的M为无色黏稠液体,易溶于水.为研究M的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| (1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)M的摩尔质量为:90g/mol. |
| (2)将此4.5g M在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | (2)M的分子式为:C3H6O3. |
| (3)通过M的红外光谱图发现该分子中既有羟基,还有羧基(--COOH) | (3)写出M中含有官能团羟基的电子式: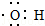 |
(4)M的核磁共振氢谱如图: | (4)M中含有4种氢原子. |
(5)综上所述,M的结构简式为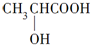 . . | |
16.如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断下列叙述不正确的是( )
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6.-2 | -1 | -1 |
| A. | 气态氢化物的稳定性HG>HF>H2E | |
| B. | B2+、D3+、E2-、G-四种离子的核外电子排布相同 | |
| C. | A、E元素与氧元素可以形成三种常见的含氧酸盐 | |
| D. | F、G元素的氢化物沸点G>F |
15.“氢能”将是未来最理想的新能源.工业上常用H2与N2合成氨气,其热化学反应方程式如下:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol-1,在某密闭容器中,将1mol的氮气与过量的氢气充分混合反应后,放出的热量为( )
| A. | 一定小于92.4kJ | B. | 一定等于92.4kJ | C. | 可能大于92.4kJ | D. | 都有可能 |
11.下列叙述正确的是( )
| A. | 汽油、柴油和地沟油都是碳氢化合物 | |
| B. | 石油的分馏和煤的干馏都是化学变化 | |
| C. | 苯环内含有碳碳单键和碳碳双键 | |
| D. | 纤维素、淀粉、蛋白质在一定条件下都能发生水解反应 |
10.下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的是Na,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(3)写出物质的电子式:①的氢化物 .
.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(3)写出物质的电子式:①的氢化物
 .
.
9.某化学反应2A?B+D在四种不同条件下进行,B、D起始浓度均为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内A的平均速率为0.013mol/(L•min).
(2)在实验2,A的初始浓度c2=1.0mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、=、<)
(4)比较实验4和实验1,可推测该反应是吸热反应(选填吸热、放热).请简述理由温度升高时,平衡向右移动.
0 156386 156394 156400 156404 156410 156412 156416 156422 156424 156430 156436 156440 156442 156446 156452 156454 156460 156464 156466 156470 156472 156476 156478 156480 156481 156482 156484 156485 156486 156488 156490 156494 156496 156500 156502 156506 156512 156514 156520 156524 156526 156530 156536 156542 156544 156550 156554 156556 156562 156566 156572 156580 203614
| 实验序号 |  | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1,反应在10至20分钟时间内A的平均速率为0.013mol/(L•min).
(2)在实验2,A的初始浓度c2=1.0mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、=、<)
(4)比较实验4和实验1,可推测该反应是吸热反应(选填吸热、放热).请简述理由温度升高时,平衡向右移动.