6.请回答下列问题:
(1)N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
则该元素是Al(填写元素符号).N原子的价电子排布图为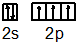 .
.
(2)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为15NA;
(3)K3[Fe(CN)6]可用来检验Fe2+,向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是产生蓝色沉淀,与CN-互为等电子体的微粒有CO、N2等(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为N>O>C;三种元素形成的简单氢化物分子中键角由大到小依次为CH4>NH3>H2O(用分子式表示).
(4)已知Fe的相对原子质量为M,阿佛加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3.则M=$\frac{32ρ{a}^{3}{N}_{A}}{3\sqrt{3}}$(用ρ、a、NA表达式表示)
(1)N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| Im/kJ•mol-1 | 578 | 1817 | 2745 | 11578 | … |
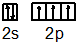 .
.(2)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为15NA;
(3)K3[Fe(CN)6]可用来检验Fe2+,向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是产生蓝色沉淀,与CN-互为等电子体的微粒有CO、N2等(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为N>O>C;三种元素形成的简单氢化物分子中键角由大到小依次为CH4>NH3>H2O(用分子式表示).
(4)已知Fe的相对原子质量为M,阿佛加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3.则M=$\frac{32ρ{a}^{3}{N}_{A}}{3\sqrt{3}}$(用ρ、a、NA表达式表示)
5.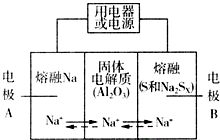 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$ 2Na+XS (3<X<5)
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$ 2Na+XS (3<X<5)
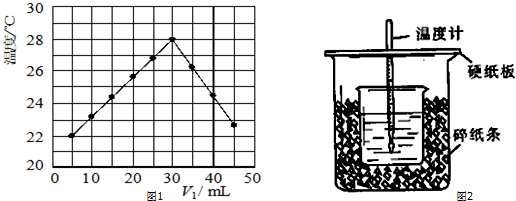
(1)根据上表数据,判断该电池工作的适宜温度应为C(填字母序号).
A.100℃以下 B.100℃~300℃
C.300℃~350℃D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1 NaCl溶液,当溶液的pH变为l3时(忽略电解前后溶液的体积变化),电路中通过的电子的物质的量为0.05mol,钠硫电池两极的反应物的质量差为2.3 g.(假设电解前钠硫电池两极的反应物质量相等)
 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$ 2Na+XS (3<X<5)
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$ 2Na+XS (3<X<5)| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
A.100℃以下 B.100℃~300℃
C.300℃~350℃D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1 NaCl溶液,当溶液的pH变为l3时(忽略电解前后溶液的体积变化),电路中通过的电子的物质的量为0.05mol,钠硫电池两极的反应物的质量差为2.3 g.(假设电解前钠硫电池两极的反应物质量相等)
4.W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,X的气态氢化物可与其最高价含氧酸反应生成盐,由此可知( )
| W | X | |
| Y | Z |
| A. | Z元素氧化物对应水化物的酸性一定强于Y | |
| B. | X、Y、W中最简单氢化物稳定性最强的是X | |
| C. | 四种元素至少有一种为金属元素 | |
| D. | 最简单氢化物的沸点:X<Y |
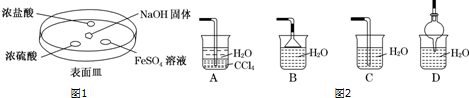
3.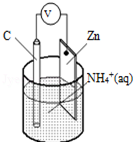 酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
 酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )| A. | 碳为电池的负极 | B. | 氨气在碳棒上生成 | ||
| C. | 电流由锌极流向碳极 | D. | H2在Zn片上生成 |
2.已知115号元素的一种核素为289X,下列有关叙述正确的是( )
| A. | 115号元素可显+5价 | B. | X原子的中子数与电子数之差为174 | ||
| C. | 115号元素位于周期表第八周期 | D. | 115号元素属于非金属元素 |
1.短周期元素X和元素Y位于不同的周期,元素X原子的最外层电子数为a,次外层电子数为b;元素Y原子的M层电子数为(a-b),L层电子数为(a+b),则关于X、Y两元素形成的化合物的说法正确的是( )
| A. | 属于两性氧化物 | B. | 能与氢氧化钠反应 | ||
| C. | 能与硫酸反应 | D. | 常温下能溶于水 |
20.下列叙述正确的是( )
| A. | Fe 与S混合加热生成FeS | |
| B. | Fe与Cl2反应生成FeCl2 | |
| C. | 过量的铜与浓硝酸反应有一氧化氮生成 | |
| D. | 氯气具有漂白性 |
19.下列各组气体,在通常条件下能稳定共存的是( )
0 156385 156393 156399 156403 156409 156411 156415 156421 156423 156429 156435 156439 156441 156445 156451 156453 156459 156463 156465 156469 156471 156475 156477 156479 156480 156481 156483 156484 156485 156487 156489 156493 156495 156499 156501 156505 156511 156513 156519 156523 156525 156529 156535 156541 156543 156549 156553 156555 156561 156565 156571 156579 203614
| A. | NH3、O2、HCl | B. | N2、H2、HCl | C. | CO2、NO、O2 | D. | H2S、O2、SO2 |