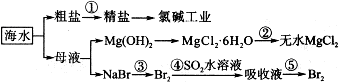
2.某实验室小组偶然发现将镁条插入饱和NaHCO3溶液中,镁条表面出现大量气泡.为了探究产生此现象的原因,该小组设计实验探究如下:
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程在烧杯中加入足量碳酸氢钠固体,加入适量蒸馏水,加热使之溶解,冷却后取上层清液即可.饱和NaHCO3溶液pH=8.4,用离子方程式表示HCO3-+H2O?H2CO3+OH-.
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同.表中不要留空格):
(3)对于反应②中产生的气体(不考虑水蒸气),请你完成假设二和假设三:
假设一:只有CO2;假设二:只有H2;假设三:H2和CO2
为检验其中是否含有CO2,写出实验步骤和结论.
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程在烧杯中加入足量碳酸氢钠固体,加入适量蒸馏水,加热使之溶解,冷却后取上层清液即可.饱和NaHCO3溶液pH=8.4,用离子方程式表示HCO3-+H2O?H2CO3+OH-.
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同.表中不要留空格):
序号 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 将镁条投入5ml蒸馏水 | 微量气泡 | |
| 2 | 将镁条投入5ml饱和NaHCO3溶液中 | Mg与NaHCO3溶液剧烈反应 | |
| 3 | 将镁条投入5ml pH=8.4NaOH溶液中 | 现象不明显 | Mg与NaOH溶液较难反应 |
假设一:只有CO2;假设二:只有H2;假设三:H2和CO2
为检验其中是否含有CO2,写出实验步骤和结论.
实验步骤 | 想象和结论 |
| 大试管中加入擦去氧化膜的镁条 加入碳酸氢钠饱和溶液,用湿润的红色石蕊试纸在锥形瓶口检验 | 若试纸变红,气体中有CO2若试纸不变红,气体中无CO2 |
1.X、Y、Z、M为构成生命体的基本元素,其原子序数依次增大,下列说法正确的是( )
| A. | 四种元素中离子半径最大的为M | |
| B. | Y、Z、M的氢化物中,M的氢化物沸点最高 | |
| C. | 四种元素最多可形成两种盐 | |
| D. | 由四种元素中的两种形成的相对分子质量最小的有机物,不能发生加成反应 |
19. 纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
(1)有研究表明阳极氧化法成功制得了Cu2O 纳米阵列,装置如图:该电池的阳极反应方程式为2Cu-2e-+2OH-=Cu2O+H2O离子交换膜为阴(填阳或阴)离子交换膜,铜网应连接电源的正极.
(2)在高温下用甲烷将粉状CuO 还原也可制得Cu2O.
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s);△H=-169kJ•mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-846.3kJ•mol-1
③Cu(s)+$\frac{1}{2}$O2(g)=CuO(s);△H=-157kJ•mol-1
则该反应的热化学方程式是:8CuO(s)+CH4(g)=4Cu2O(s)+CO2(g)+2H2O(g)△H=-266.3kJ/mol.
(3)在相同的密闭容器中,用等质量的三种纳米Cu2O(用不同方法制得)分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0.水蒸气浓度随时间t变化如下表所示:
①对比实验的温度:T2>T1(填“>”“<”或“﹦”),原因是因为该反应的正反应方向为吸热方向,升温,平衡正向移动,平衡常数增大,③的平衡常数大于①,说明T2大于T1.
②实验①前20min的平均反应速率 v(O2)=3.5×10-5mol/(L•min)
③比较不同方法制得的Cu2O的催化效果应选用①和②组实验,原因是除催化剂外,其他条件相同.
 纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.(1)有研究表明阳极氧化法成功制得了Cu2O 纳米阵列,装置如图:该电池的阳极反应方程式为2Cu-2e-+2OH-=Cu2O+H2O离子交换膜为阴(填阳或阴)离子交换膜,铜网应连接电源的正极.
(2)在高温下用甲烷将粉状CuO 还原也可制得Cu2O.
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s);△H=-169kJ•mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-846.3kJ•mol-1
③Cu(s)+$\frac{1}{2}$O2(g)=CuO(s);△H=-157kJ•mol-1
则该反应的热化学方程式是:8CuO(s)+CH4(g)=4Cu2O(s)+CO2(g)+2H2O(g)△H=-266.3kJ/mol.
(3)在相同的密闭容器中,用等质量的三种纳米Cu2O(用不同方法制得)分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0.水蒸气浓度随时间t变化如下表所示:
| 序号 |  | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
②实验①前20min的平均反应速率 v(O2)=3.5×10-5mol/(L•min)
③比较不同方法制得的Cu2O的催化效果应选用①和②组实验,原因是除催化剂外,其他条件相同.
17. 常温下,向20mL0.1mol/L某酸HR溶液中滴加0.1mol/L氢氧化钠溶液,溶液的PH与氢氧化钠溶液体积V的关系如图所示.下列说法不正确的是( )
常温下,向20mL0.1mol/L某酸HR溶液中滴加0.1mol/L氢氧化钠溶液,溶液的PH与氢氧化钠溶液体积V的关系如图所示.下列说法不正确的是( )
 常温下,向20mL0.1mol/L某酸HR溶液中滴加0.1mol/L氢氧化钠溶液,溶液的PH与氢氧化钠溶液体积V的关系如图所示.下列说法不正确的是( )
常温下,向20mL0.1mol/L某酸HR溶液中滴加0.1mol/L氢氧化钠溶液,溶液的PH与氢氧化钠溶液体积V的关系如图所示.下列说法不正确的是( )| A. | 可选酚酞或甲基橙作指示剂 | |
| B. | 滴定前HR溶液中存在大量HR分子 | |
| C. | V=20 mL时,溶液中水电离的:c(H+)×c(OH-)=1×10-14mol2/L2 | |
| D. | c点时溶液中离子浓度大小关系有c(Na+)>c(R-)>c(OH-)>c(H+) |
15.青蒿素是一种有效的抗疟药.常温下,青蒿素为无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157℃.提取青蒿素的方法之一是乙醚浸取法,提取流程如图1:
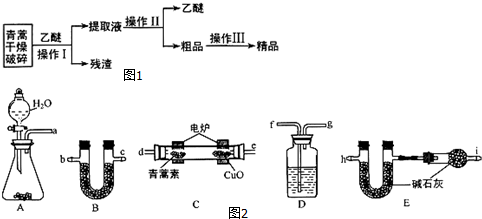
请回答下列问题:
(1)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作Ⅰ用到的玻璃仪器是漏斗、玻璃棒、烧杯,操作Ⅱ的名称是蒸馏.
(3)用如图2的实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
①仪器各接口的连接顺序从左到右依次为afgdebchi(每个装置限用一次).
②装置C中CuO的作用是使青蒿素充分氧化生成CO2和H2O.
③装置D中的试剂为浓硫酸.
④已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
则青蒿素的最简式为C15H22O5.
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是C(填字母代号).
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.
0 156358 156366 156372 156376 156382 156384 156388 156394 156396 156402 156408 156412 156414 156418 156424 156426 156432 156436 156438 156442 156444 156448 156450 156452 156453 156454 156456 156457 156458 156460 156462 156466 156468 156472 156474 156478 156484 156486 156492 156496 156498 156502 156508 156514 156516 156522 156526 156528 156534 156538 156544 156552 203614

请回答下列问题:
(1)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作Ⅰ用到的玻璃仪器是漏斗、玻璃棒、烧杯,操作Ⅱ的名称是蒸馏.
(3)用如图2的实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
①仪器各接口的连接顺序从左到右依次为afgdebchi(每个装置限用一次).
②装置C中CuO的作用是使青蒿素充分氧化生成CO2和H2O.
③装置D中的试剂为浓硫酸.
④已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是C(填字母代号).
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.
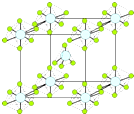 磷元素在生产和生活中有广泛的应用.
磷元素在生产和生活中有广泛的应用.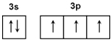 .
.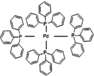 ):P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为sp3;判断该物质在水中溶解度并加以解释不易溶于水.水为极性分子,四(三苯基膦)钯分子为非极性分子,分子极性不相似,故不相溶.该物质可用于如图所示物质A(
):P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为sp3;判断该物质在水中溶解度并加以解释不易溶于水.水为极性分子,四(三苯基膦)钯分子为非极性分子,分子极性不相似,故不相溶.该物质可用于如图所示物质A(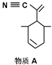 )的合成:物质A中碳原子杂化轨道类型为sp、sp2、sp3;一个A分子中手性碳原子数目为3.
)的合成:物质A中碳原子杂化轨道类型为sp、sp2、sp3;一个A分子中手性碳原子数目为3.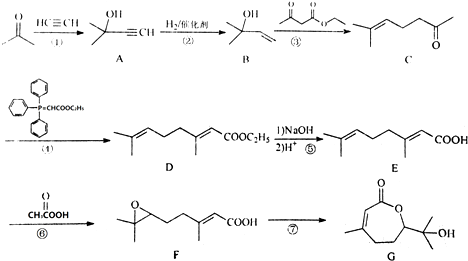
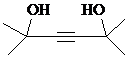 .
.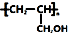 ,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.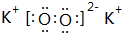 .
.