2.化学与生活、社会发展息息相关,下列有关说法与氧化还原反应无关的是( )
| A. | KNO3、KClO3与单质S、C2H5OH不能混搭存放在同一库房间 | |
| B. | 缺铁性补血服用补铁剂时,需与维C同时服用 | |
| C. | 铜制品、铁制品在潮湿的空气中生锈 | |
| D. | 用乙醚从黄花蒿中提取青蒿素 |
20.下列表示除去X中所含杂质的过程.下列方案不能达到目的是( )
X(含杂质)$→_{操作②}^{加入①}$X
X(含杂质)$→_{操作②}^{加入①}$X
| 选项 | X(括号中的物质为杂质) | ① | ② |
| A | 乙酸乙酯(乙醇) | 饱和碳酸钠溶液 | 萃取、分液 |
| B | BaSO4(BaSO3) | 稀硝酸 | 过滤 |
| C | NaCl(Na2CO3) | 盐酸 | 蒸发结晶 |
| D | 铜(铝) | 浓硫酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
19.X、Y、Z、W为原子序数依次增大的短周期主族元素,X元素的一种原子不含中子,Y元素在大气中存在两种常见单质,Z与X处于同一主族,W原子最外层电子数是次外层电子数的0.875倍.下列叙述正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | 最简单氢化物的沸点:Y>W | |
| C. | 化合物Z2Y2与X2Y2中化学键完全相同 | |
| D. | 由Y、Z、W三种元素组成的化合物的水溶液一定显中性 |
18.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,28 g 14CO和N2的混合物所含的质子数为14NA | |
| B. | 常温下,100 mL 1 mol•L-1Na2CO3溶液中阴离子总数大于0.1 NA | |
| C. | 将NA个NH3分子溶于1 L水中得到1 mol•L-1的氨水 | |
| D. | 1 mol Cl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA |
17.屠呦呦因发现了青蒿素这种抗疟良药而获得2015年诺贝尔奖,这充分说明了“化学让人们生活更美好”.下列不属于化学反应在生活中的应用的是( )
| A. | 将氧化铁添加到油漆中制红色油漆 | B. | 用氯气给自来水消毒 | ||
| C. | 将粘土烧制成精美的瓷器 | D. | 用食醋清洗水壶中的水垢 |
16.决定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
A通常显+3价,B元素的核外电子排布式为1s22s22p63s2.
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3.
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),已知3种离子晶体的晶格能数据如下表:
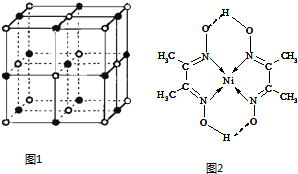
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是TiN>MgO>CaO>KCl.
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.FeCl3和CuCl2中,适合作录音带磁粉原料的是FeCl3.
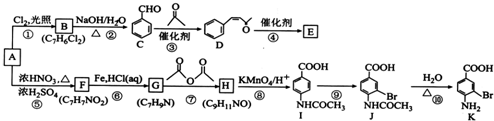
(5)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3.
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.FeCl3和CuCl2中,适合作录音带磁粉原料的是FeCl3.
(5)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键.
14.下列对有关化工生产的说法正确的是( )
0 156341 156349 156355 156359 156365 156367 156371 156377 156379 156385 156391 156395 156397 156401 156407 156409 156415 156419 156421 156425 156427 156431 156433 156435 156436 156437 156439 156440 156441 156443 156445 156449 156451 156455 156457 156461 156467 156469 156475 156479 156481 156485 156491 156497 156499 156505 156509 156511 156517 156521 156527 156535 203614
| A. | 合成氨生产过程中将NH3液化分离,可以提高反应物的转化率 | |
| B. | 硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 | |
| C. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阳极室产生的Cl2进入阴极室 | |
| D. | 传统硅酸盐工业中生产水泥的原料为石灰石、纯碱和石英砂 |
 .
.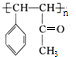 .
.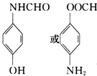 .
.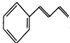 的合成路线补充完整.
的合成路线补充完整.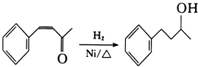 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$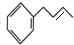 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$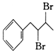 $→_{△}^{NaOH醇溶液}$
$→_{△}^{NaOH醇溶液}$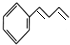 (无机试剂及溶剂任选).
(无机试剂及溶剂任选).
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等. ;用化学方程式表示工业上常用于冶炼T单质的原理是2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
;用化学方程式表示工业上常用于冶炼T单质的原理是2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑; ;
;