15.用铝箔包裹着2.3g金属钠,投入到足量水中,产生的氢气的质量为0.16g,则铝箔的质量为( )
| A. | 0.45 g | B. | 0.54 g | C. | 0.5 g | D. | 0.35 g |
14. A、B、D、E、F是原子序数依次增大的五种前四周期元素,相关信息如下:
A、B、D、E、F是原子序数依次增大的五种前四周期元素,相关信息如下:
(1)D元素是氮(填元素名称);D、E两元素第一电离能较大的是N(填元素符号);原因是氮元素原子2p轨道为半满稳定状态,能量较低,第一电离能大于元素的.
(2)B、D元素分别与A元素形成的最简单分子的VSERP模型分别为四面体形、四面体形(用文字描述),两者沸点较高的是NH3(填化学式),原因是氨气分子之间形成氢键,而甲烷分子之间不能形成氢键.
(3)F元素基态原子价电子排布图为 ,能量最高的电子占据的能级符号为3d,该能级所在能层具有的原子轨道数为9.
,能量最高的电子占据的能级符号为3d,该能级所在能层具有的原子轨道数为9.
(4)D、F形成的一种晶体,晶胞如图所示,该晶体化学式为TiN.已知晶体的密度为ρ g•cm-3,阿伏伽德罗常数为NA,则晶胞边长为$\root{3}{\frac{248}{ρ{N}_{A}}}$×1010pm.
 A、B、D、E、F是原子序数依次增大的五种前四周期元素,相关信息如下:
A、B、D、E、F是原子序数依次增大的五种前四周期元素,相关信息如下:| A | 原子半径最小的元素 |
| B | 原子核外电子有6种不同的运动状态 |
| E | 原子L电子层上有两个未成对电子 |
| F | 原子最外层有2个电子,次外层电子数为D原子最外层电子数的2倍 |
(2)B、D元素分别与A元素形成的最简单分子的VSERP模型分别为四面体形、四面体形(用文字描述),两者沸点较高的是NH3(填化学式),原因是氨气分子之间形成氢键,而甲烷分子之间不能形成氢键.
(3)F元素基态原子价电子排布图为
 ,能量最高的电子占据的能级符号为3d,该能级所在能层具有的原子轨道数为9.
,能量最高的电子占据的能级符号为3d,该能级所在能层具有的原子轨道数为9.(4)D、F形成的一种晶体,晶胞如图所示,该晶体化学式为TiN.已知晶体的密度为ρ g•cm-3,阿伏伽德罗常数为NA,则晶胞边长为$\root{3}{\frac{248}{ρ{N}_{A}}}$×1010pm.
13.把足量的铁粉投入到硫酸与硫酸铜的混合溶液中,充分反应后,残余固体的质量与原来加入的铁粉的质量相等,则原溶液中H+和SO42-的物质的量之比为( )
| A. | 1:4 | B. | 2:7 | C. | 1:2 | D. | 8:3 |
12.下列含有非极性键的化合物是( )
0 156327 156335 156341 156345 156351 156353 156357 156363 156365 156371 156377 156381 156383 156387 156393 156395 156401 156405 156407 156411 156413 156417 156419 156421 156422 156423 156425 156426 156427 156429 156431 156435 156437 156441 156443 156447 156453 156455 156461 156465 156467 156471 156477 156483 156485 156491 156495 156497 156503 156507 156513 156521 203614
| A. | MgCl2 | B. | Na2O2 | C. | H2O | D. | N2 |
 .
. .
.
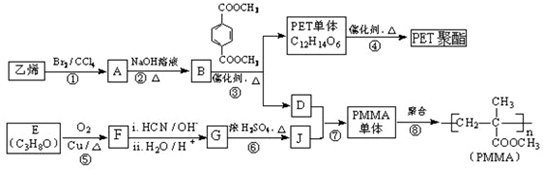
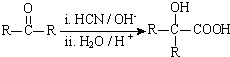 (R、R′代表烃基)
(R、R′代表烃基)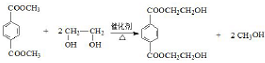 ;
; ;
;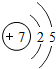 ;
;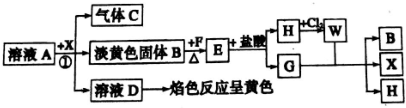
 ,G中化学键的类型为极性共价键;
,G中化学键的类型为极性共价键;