7.①~⑨是元素周期表中的部分元素.
请回答:
(1)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式是OH-+Al(OH)3=AlO2-+2H2O.
(2)用电子式表示元素⑥和⑨形成的化合物的过程 .
.
(3)某同学为了比较元素②和硅元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验).请回答:
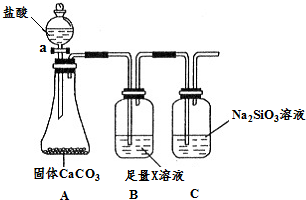
a.X是NaHCO3(填化学式),B装置的作用是吸收二氧化碳中混有的HCl气体.
b.能说明元素②和硅元素非金属性强弱的实验现象是C中产生白色胶状沉淀,相关的化学方程式是:CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓.
(4)请设计实验比较元素⑥与⑦金属性的相对强弱取一小段镁条和一小片铝片,磨去表面氧化膜,分别放入2支试管中,各加入等体积等浓度的盐酸,观察发生的现象.
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | |||||||
(1)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式是OH-+Al(OH)3=AlO2-+2H2O.
(2)用电子式表示元素⑥和⑨形成的化合物的过程
 .
.(3)某同学为了比较元素②和硅元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验).请回答:

a.X是NaHCO3(填化学式),B装置的作用是吸收二氧化碳中混有的HCl气体.
b.能说明元素②和硅元素非金属性强弱的实验现象是C中产生白色胶状沉淀,相关的化学方程式是:CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓.
(4)请设计实验比较元素⑥与⑦金属性的相对强弱取一小段镁条和一小片铝片,磨去表面氧化膜,分别放入2支试管中,各加入等体积等浓度的盐酸,观察发生的现象.
6.下列各组微粒中,电子总数相同的是( )
| A. | F-、Cl-、Br-、I- | B. | S2-、Ca2+、Ar、Cl- | ||
| C. | Na+、K+、Mg2+、Al3+ | D. | Mg2+、Mg、Al3+、Al |
4.下列反应的离子方程式中不正确的是( )
| A. | 碳酸钙中滴入盐酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | Fe(OH)3 中滴入硫酸 OH-+H +═H2O | |
| C. | AgNO3中滴入NaCl溶液 Ag ++Cl-═AgCl↓ | |
| D. | CO2通入到足量NaOH溶液中CO2+2OH-═CO32-+H2O |
19.将下图所列仪器组装成一套实验室蒸馏石油的装置,并进行蒸馏得到汽油和煤油.
(1)上图中A、B、两种仪器的名称分别是冷凝管;蒸馏烧瓶;
(2)A仪器中,c口是进水口,
(3)蒸馏时,温度计水银球应在蒸馏烧瓶支管口位置.
(4)在B中注入原油后,再加几片碎瓷片的目的是防止暴沸.
0 156316 156324 156330 156334 156340 156342 156346 156352 156354 156360 156366 156370 156372 156376 156382 156384 156390 156394 156396 156400 156402 156406 156408 156410 156411 156412 156414 156415 156416 156418 156420 156424 156426 156430 156432 156436 156442 156444 156450 156454 156456 156460 156466 156472 156474 156480 156484 156486 156492 156496 156502 156510 203614
| 三 | 一 | 五 | 二 | 六 | 四 |
 |  |  |  |  |  |
(2)A仪器中,c口是进水口,
(3)蒸馏时,温度计水银球应在蒸馏烧瓶支管口位置.
(4)在B中注入原油后,再加几片碎瓷片的目的是防止暴沸.
 .
. .
. ;
;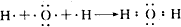 ;
;