20.下列说法中不正确的是( )
| A. | 所有单键均有σ键 | B. | 双键、三键中必有σ键与π键 | ||
| C. | σ键、π键都可以绕轴自由旋转 | D. | π键不如σ键牢固 |
19.根据等电子原理,下列各组分子或离子的空间构型不相似的是( )
| A. | NH4+和CH4 | B. | H3O+和NH3 | C. | NO3-和CO32- | D. | CO2和H2O |
17.已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | 金属性:B>A,非金属性:D>C |
16.在可逆反应mX+nY?pZ+qW中,在反应开始后的10s,若用每种物质的浓度增加表示该段时间的平均反应速率时分别为v(X=0.5amol•L-1•s-1,v(Y)=0.25amol•L-1•s-1,v(Z)=amol•L-1•s-1,v(W)=1.5amol•L-1•s-1.若用每种物质的浓度减少表示该段时间的平均反应速率时分别为v(X)=amol•L-1•s-1,v(Y)=0.5amol•L-1•s-1,v(Z)=0.5amol•L-1•s-1,v(W)=0.75amol•L-1•s-1,则m:n:p:q为( )
| A. | 2:1:2:3 | B. | 2:1:4:6 | C. | 2:1:4:3 | D. | 1:1:1:1 |
12.下列实验现象正确的是( )
0 156287 156295 156301 156305 156311 156313 156317 156323 156325 156331 156337 156341 156343 156347 156353 156355 156361 156365 156367 156371 156373 156377 156379 156381 156382 156383 156385 156386 156387 156389 156391 156395 156397 156401 156403 156407 156413 156415 156421 156425 156427 156431 156437 156443 156445 156451 156455 156457 156463 156467 156473 156481 203614
| 实验现象 | 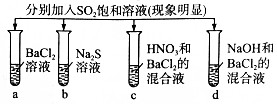 | |||
| A | 白色沉淀 | 臭鸡蛋气味气体 | 无色溶液 | 无色溶液 |
| B | 无色溶液 | 无色无味气体 | 白色沉淀 | 白色沉淀 |
| C | 无色溶液 | 浅黄色沉淀 | 白色沉淀 | 白色沉淀 |
| D | 白色沉淀 | 浅黄色沉淀 | 无色溶液 | 无色溶液 |
| A. | A | B. | B | C. | C | D. | D |
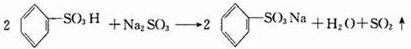 、③
、③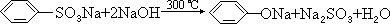 、④
、④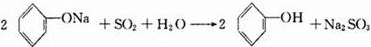 .
.
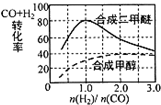 碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应:
碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应: