9.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,78g Na2O2的分子数为NA | |
| B. | 标准状况下,22.4L氯气在任何反应中转移电子数均为2NA | |
| C. | 标准状况下,22.4mL H2O中含水分子的个数约为1.24NA | |
| D. | 17g NH3溶于水后溶质NH3的个数为NA |
8.下列分子中的各原子均在同一平面上的是( )
| A. | C2H3Cl | B. | CHCl3 | C. | CH3CH═CH2 | D. | CH3-CH3 |
7.某化学兴趣小组根据部分物质的性质,设计了以下的实验流程:
①Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3
②S$\stackrel{O_{2}/点燃}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO3
③Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3$\stackrel{△}{→}$无水FeCl3
下列判断正确的是( )
①Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3
②S$\stackrel{O_{2}/点燃}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO3
③Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3$\stackrel{△}{→}$无水FeCl3
下列判断正确的是( )
| A. | 步骤①②中的SO2气体和CO2气体可以用澄清石灰水溶液鉴别 | |
| B. | 步骤③中,检验FeCl3(aq)溶液中是否存有Fe2+,应该选用KSCN溶液 | |
| C. | 三个步骤中都没有氧化还原反应 | |
| D. | 常温下,H2SO3溶液中通入少量氯气,溶液pH减小,Kw不变 |
6.已知H2O2的分子结构可表示为H-O-O-H,设H2O2中H、O两元素是由${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{8}^{16}$O、${\;}_{8}^{18}$O四种核素组成,则共有H2O2分子的种类是( )
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
3.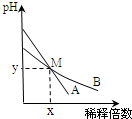 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )| A. | 稀释前,c(A)=10c(B) | |
| B. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L | |
| C. | 用醋酸中和A溶液至恰好完全反应时,溶液的pH为7 | |
| D. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 |
2.下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
| A. | 等物质的量浓度的下列溶液:①H2CO3、②Na2CO3、③NaHCO3、④(NH4)2CO3:其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3 溶液中加入等体积0.1 mol•L-1NaOH 溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
1.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
0 156286 156294 156300 156304 156310 156312 156316 156322 156324 156330 156336 156340 156342 156346 156352 156354 156360 156364 156366 156370 156372 156376 156378 156380 156381 156382 156384 156385 156386 156388 156390 156394 156396 156400 156402 156406 156412 156414 156420 156424 156426 156430 156436 156442 156444 156450 156454 156456 156462 156466 156472 156480 203614
| A. | 标准状况下,22.4L臭氧与22.4L氢气所含原子数均为2NA | |
| B. | 46gNO2和N2O4的混合气体中含有的原子数为3NA | |
| C. | 2.24LCH4所含电子数为NA | |
| D. | 1molO2参加反应转移的电子数一定为4NA |