10.短周期元素X、Y、Z、W在周期表中位置如图所示.已知Y、W的原子序数之和是Z 的3倍,下列说法正确的是( )
| Y | Z | ||
| X | W |
| A. | 原子半径:Z>Y>X | B. | 气态氢化物的稳定性:X>Z | ||
| C. | Z、W均能与 Mg 形成离子化合物 | D. | 最高价氧化物的水化物的酸性:Y>W |
9.下列说法不正确的是( )
| A. | 早在1 000多年前,我国就已采用加热胆矾(CuSO4•5H2O)或绿矾(FeSO4•7H2O) 的方法制硫酸,尽管硫酸的生产工艺几经改进,此方法仍然是工业生产硫酸的主要方法 | |
| B. | 氢能是未来能源结构中最具发展潜力的清洁能源之一.目前已有专家研究出用淀粉或纤维素与水在酶作用下转变为二氧化碳和氢气的方法制氢气.从整个循环来看,利用该方法得到的氢能来源于太阳能 | |
| C. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 有机反应中的加聚反应符合绿色化学的原则 |
6.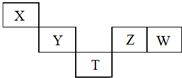 X~T元素在周期表中的相对位置如图所示,其中X、Y、Z、W元素原子的最外层电子数之和为20,T为第4周期元素.下列说法正确的是( )
X~T元素在周期表中的相对位置如图所示,其中X、Y、Z、W元素原子的最外层电子数之和为20,T为第4周期元素.下列说法正确的是( )
 X~T元素在周期表中的相对位置如图所示,其中X、Y、Z、W元素原子的最外层电子数之和为20,T为第4周期元素.下列说法正确的是( )
X~T元素在周期表中的相对位置如图所示,其中X、Y、Z、W元素原子的最外层电子数之和为20,T为第4周期元素.下列说法正确的是( )| A. | YW4与H2在高温下反应主要生成YH4和HW | |
| B. | X的原子半径比T原子半径小,两者原子序数之差为29 | |
| C. | W氧化物的水化物的酸性一定强于Z的氧化物的水化物 | |
| D. | T的氢化物可能具有强的还原性,其稳定性小于Z的氢化物 |
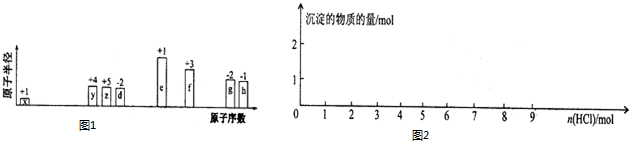
4.实验室使用pH传感器来测定Na2CO3和NaHCO3混合溶液中NaHCO3的含量.取该混合溶液25.00mL,用0.1mol•L-1盐酸进行滴定,得到如下曲线.以下说法正确的是( )
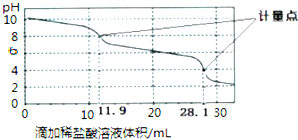

| A. | 此样品中NaHCO3的物质的量为(28.1-11.9)×10-4mol | |
| B. | 整个滴定过程中,溶液中阴离子总数始终不变 | |
| C. | 滴加稀盐酸的体积为11.90mL时:c(H+)+c(H2CO3)═c(OH-)+c(CO32-) | |
| D. | 该方法无法测定Na2CO3和NaOH混合溶液中NaOH的含量 |
3.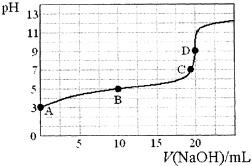 已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
 已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+ | |
| B. | 常温下,Ka(H3PO2)≈10-5 | |
| C. | 该滴定实验中,用酚酞作指示剂比用甲基橙作指示剂的误差小 | |
| D. | B点溶液中存在关系:c(H+)+c(H3PO2)=c(OH-)+c(H2PO2-) |
2.下列物质的制备原理设计步骤合理的是( )
0 156278 156286 156292 156296 156302 156304 156308 156314 156316 156322 156328 156332 156334 156338 156344 156346 156352 156356 156358 156362 156364 156368 156370 156372 156373 156374 156376 156377 156378 156380 156382 156386 156388 156392 156394 156398 156404 156406 156412 156416 156418 156422 156428 156434 156436 156442 156446 156448 156454 156458 156464 156472 203614
| A. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$ H2SO4 | |
| B. | Fe $→_{点燃}^{Cl_{2}}$ FeCl2$\stackrel{NaOH溶液}{→}$ Fe(OH)2 | |
| C. | AlCl3(溶液)$\stackrel{蒸发}{→}$ AlCl3$\stackrel{电解}{→}$ Al | |
| D. | NaCl(饱和溶液)$\stackrel{依次通入NH_{3}、CO_{2}}{→}$ NaHCO3$\stackrel{△}{→}$Na2CO3 |
 .
.
 .
.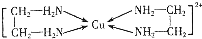 第四周期金属Cr、Fe、Cu在科学研究和工业生产中都有重要的用途.请回答下列问题:
第四周期金属Cr、Fe、Cu在科学研究和工业生产中都有重要的用途.请回答下列问题: