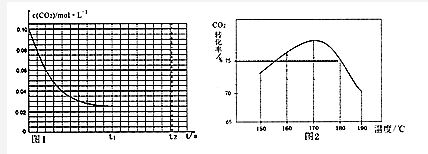
16.卤素的单质和化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
回答下列问题:
(1)溴原子的价层电子排布图为 .根据下表提供的第一电离能数,据判断,最有可能生成较稳定的单核阳离子的卤素原子是I
.根据下表提供的第一电离能数,据判断,最有可能生成较稳定的单核阳离子的卤素原子是I
(2)氢氟酸在一定浓度的溶液中主要以二分子缔合(HF)2形式存在,使氟化氢分子缔合的相互作用是氢键.碘在水中溶解度小,但在碘化钾溶液中明显增大,这是由于发生反应:I+I2=I3-,CsICl2与KI3类似,受热易分解,倾向于生成晶格能更大的物质,试写出CsICl2受热分解的化学方程式:CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsCl+ICl.
(3)ClO2-中心氯原子的杂化轨道类型为sp3,与ClO2-具有相同空间构型和键合形式的物质化学式为(写出一个即可)Cl2O、OF2等.
(4)如图1为碘晶体胞结构,平均每个晶胞中有8个碘原子,碘晶体中碘分子的配位数为12.
(5)已知NA为阿伏加德罗常数,CaF2晶体密度为ρg•cm-3,其晶胞如图2所示,两个最近Ca2+核间距离为anm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$×10-21a3ρNA.

回答下列问题:
(1)溴原子的价层电子排布图为
 .根据下表提供的第一电离能数,据判断,最有可能生成较稳定的单核阳离子的卤素原子是I
.根据下表提供的第一电离能数,据判断,最有可能生成较稳定的单核阳离子的卤素原子是I| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ•mol-1) | 1681 | 1251 | 1140 | 1008 |
(3)ClO2-中心氯原子的杂化轨道类型为sp3,与ClO2-具有相同空间构型和键合形式的物质化学式为(写出一个即可)Cl2O、OF2等.
(4)如图1为碘晶体胞结构,平均每个晶胞中有8个碘原子,碘晶体中碘分子的配位数为12.
(5)已知NA为阿伏加德罗常数,CaF2晶体密度为ρg•cm-3,其晶胞如图2所示,两个最近Ca2+核间距离为anm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$×10-21a3ρNA.

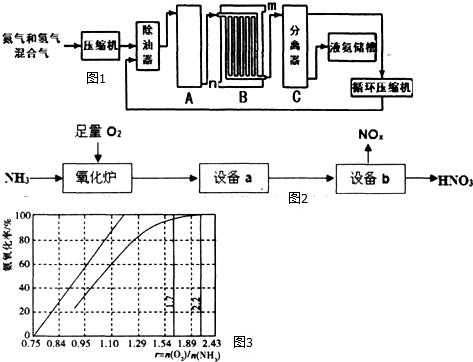
14.由水钴矿[主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等]制取CoCl2•6H2O的工艺流程如下:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
③CoCl2•6H2O熔点为86℃,加热至110-120℃时,失去结晶水生成CoCl2.
回答下列问题:
(1)浸出过程中Co2O3发生反应的化学方程式为Co2O3+Na2SO3+4HCl=2CoCl2+Na2SO4+2H2O
(2)NaClO3在浸出液中发生反应的离子方程式为ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O
(3)“加Na2CO3调pH至5.2”,过滤所得滤渣的主要成分为Fe(OH)3、Al(OH)3(填化学式).
(4)萃取剂对金属离子的萃取与溶液pH的关系如图2所示,向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B(填选项字母)
A.2.0-2.5 B.3.0-3.5C.4.0-4.5 D.5.0-5.5
(5)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.为测定粗产品中CoCl2•6H2O含量.称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是(写两条):①粗产品含有可溶性氯化物,②晶体失去了部分结晶水.

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
回答下列问题:
(1)浸出过程中Co2O3发生反应的化学方程式为Co2O3+Na2SO3+4HCl=2CoCl2+Na2SO4+2H2O
(2)NaClO3在浸出液中发生反应的离子方程式为ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O
(3)“加Na2CO3调pH至5.2”,过滤所得滤渣的主要成分为Fe(OH)3、Al(OH)3(填化学式).
(4)萃取剂对金属离子的萃取与溶液pH的关系如图2所示,向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+,其使用的最佳pH范围是B(填选项字母)
A.2.0-2.5 B.3.0-3.5C.4.0-4.5 D.5.0-5.5
(5)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.为测定粗产品中CoCl2•6H2O含量.称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是(写两条):①粗产品含有可溶性氯化物,②晶体失去了部分结晶水.
13.某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验.
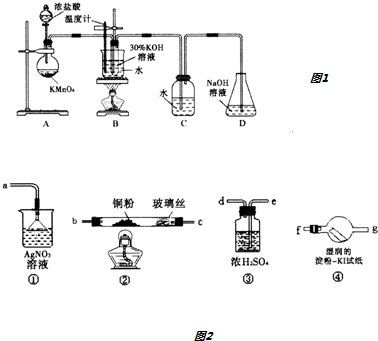
【实验一】制取氯酸钾和氯水.
利用如图1所示实验装置和药品进行实验.
(1)装置A中玻璃仪器为圆底烧瓶和分液漏斗,若对调B和C装置的位置,可能(填“可能”或“不可能”)提高B中氯酸钾的产率.
【实验二】检验上述制备Cl2中混有的HCl.
选用图1装置A和图2所给装置以及药品进行实验.
(2)实验仪器接口连接顺序为:装置A→e、d→b、c→f、g→a.
能证明HCl存在的现象是④中淀粉-KI试纸不变蓝色,装置①中产生白色沉淀.
【实验三】氯酸钾与碘化钾反应的研究.
在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
(3)系列a实验的实验目的是研究反应体系中硫酸浓度对反应产物的影响,设计1号试管实验的作用是硫酸浓度为0的对比实验.
【实验四】比较HClO与HCO3-电离常数的大小和测定饱和氯水中氯元素的总量.
查阅资料知:
i.实验室难以获得纯HClO溶液;
ii.次氯酸会破坏酸碱指示剂;
iii.次氯酸或氯气可被SO2、H2O2、和FeCl2等物质还原成Cl-.
(4)设计实验证明(实验方案不必描述操作过程的细节);
①相同条件下,HClO的电离常数大于HCO3-:配制相同物质的量浓度的碳酸钠和次氯酸钠溶液,用pH计分别测定两种溶液的pH值.
②确定饱和氯水中氯元素的总量:量取一定量的试样,加入足量的双氧水溶液,充分反应后,加热除去过量的双氧水,冷却,再加入足量的硝酸银溶液,过滤,洗净烘干后称量沉淀质量,计算可得.

【实验一】制取氯酸钾和氯水.
利用如图1所示实验装置和药品进行实验.
(1)装置A中玻璃仪器为圆底烧瓶和分液漏斗,若对调B和C装置的位置,可能(填“可能”或“不可能”)提高B中氯酸钾的产率.
【实验二】检验上述制备Cl2中混有的HCl.
选用图1装置A和图2所给装置以及药品进行实验.
(2)实验仪器接口连接顺序为:装置A→e、d→b、c→f、g→a.
能证明HCl存在的现象是④中淀粉-KI试纸不变蓝色,装置①中产生白色沉淀.
【实验三】氯酸钾与碘化钾反应的研究.
在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/ml | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
【实验四】比较HClO与HCO3-电离常数的大小和测定饱和氯水中氯元素的总量.
查阅资料知:
i.实验室难以获得纯HClO溶液;
ii.次氯酸会破坏酸碱指示剂;
iii.次氯酸或氯气可被SO2、H2O2、和FeCl2等物质还原成Cl-.
(4)设计实验证明(实验方案不必描述操作过程的细节);
①相同条件下,HClO的电离常数大于HCO3-:配制相同物质的量浓度的碳酸钠和次氯酸钠溶液,用pH计分别测定两种溶液的pH值.
②确定饱和氯水中氯元素的总量:量取一定量的试样,加入足量的双氧水溶液,充分反应后,加热除去过量的双氧水,冷却,再加入足量的硝酸银溶液,过滤,洗净烘干后称量沉淀质量,计算可得.
12.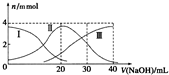 常温下,向20mlH2A溶液中滴加相同物质的量浓度NaOH溶液,有关微粒物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),下列说法正确的是( )
常温下,向20mlH2A溶液中滴加相同物质的量浓度NaOH溶液,有关微粒物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),下列说法正确的是( )
 常温下,向20mlH2A溶液中滴加相同物质的量浓度NaOH溶液,有关微粒物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),下列说法正确的是( )
常温下,向20mlH2A溶液中滴加相同物质的量浓度NaOH溶液,有关微粒物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),下列说法正确的是( )| A. | H2A在水中电离方程式为:H2A?2H++A2- | |
| B. | V(NaOH)=20ml时,溶液呈酸性 | |
| C. | V(NaOH)=30mL时,溶液中有以下关系:c(A2-)+c(H2A)+c(HA-)=c(Na+) | |
| D. | V(NaOH)=40mL时,溶液中有以下关系:c(H+)+c(HA-)+c(H2A)=c(OH-) |
11.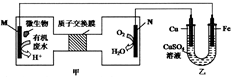 下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )
下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )
 下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )
下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )| A. | 甲中H+透过质子交换膜由左向右移动 | |
| B. | M极电极反应式:H2N(CH2)NH2+4H2O-16e-═2CO2↑+N2↑+16e- | |
| C. | 一段时间后,乙中CuSO4溶液浓度基本保持不变 | |
| D. | 当N极消耗0.25molO2时,则铁极增重16g |
10.X、Y、Z、W是原子序数逐渐增大的四种短周期主族元素,其原子半径如下表,已知Y、Z两种元素的单质是空气主要成分,W原子最外层电子数与Ne原子最外层电子数相差1.下列说法正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径/nm | 0.037 | 0.075 | 0.074 | 0.099 |
| A. | Y、Z、W处于周期表中同一周期 | B. | 通常状况下得不到纯净的YZ2 | ||
| C. | X与Z形成的化合物不含非极性键 | D. | X、Z、W形成的化合物为弱酸 |
9.对下列实验的现象描述及其解释均正确的是( )
0 156271 156279 156285 156289 156295 156297 156301 156307 156309 156315 156321 156325 156327 156331 156337 156339 156345 156349 156351 156355 156357 156361 156363 156365 156366 156367 156369 156370 156371 156373 156375 156379 156381 156385 156387 156391 156397 156399 156405 156409 156411 156415 156421 156427 156429 156435 156439 156441 156447 156451 156457 156465 203614
| 选项 | 实验 | 现象 | 解释 |
| A | 向新制氯水中滴加紫色石蕊试液 | 溶液变为红色且保持不变 | 新制氯水具有酸性 |
| B | SO2通入Ba(NO3)2溶液中 | 有白色沉淀生成 | 符合复分解反应发生条件 |
| C | 无色溶液中滴加FeCl3溶液和CCl4,振荡、静置 | 下层显紫色 | 原溶液中含有I- |
| D | 将少量酸性高锰酸钾溶液滴入乙酸溶液中 | 溶液仍为无色 | 高锰酸钾发生还原反应 |
| A. | A | B. | B | C. | C | D. | D |
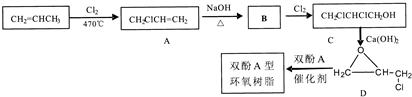
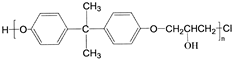
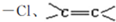 ,C的化学名称为2,3-二氯-1-丙醇.
,C的化学名称为2,3-二氯-1-丙醇.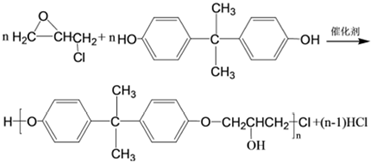
 为起始原料制备
为起始原料制备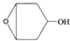 的合成路线:
的合成路线: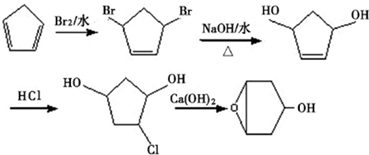 .
.