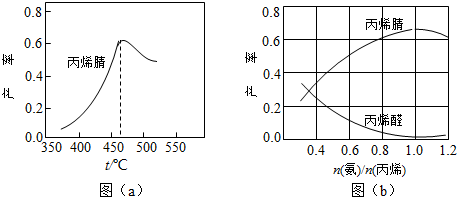
13.氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2.某同学在实验室中对NH3与NO2反应进行了探究.回答下列问题:
(1)氨气的制备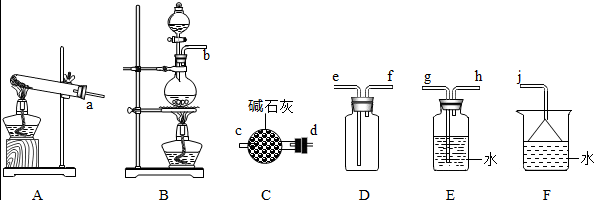
①氨气的发生装置可以选择上图中的A,反应的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→d→c→f→e→j(按气流方向,用小写字母表示).
(2)氨气与二氧化氮的反应
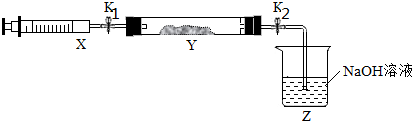
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度下按图示装置进行实验.
(1)氨气的制备

①氨气的发生装置可以选择上图中的A,反应的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→d→c→f→e→j(按气流方向,用小写字母表示).
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度下按图示装置进行实验.

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中红棕色气体慢慢变浅 | ②反应的化学方程式 8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | ③Z中NaOH溶液产生倒吸现象 | ④反应后气体分子数减少,Y管压强小于外压 |
12.298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )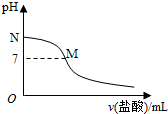

| A. | 该滴定过程应该选择酚酞作为指示剂 | |
| B. | M点对应的盐酸体积为20.0mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
11.下列实验操作能达到实验目的是( )
| A. | 用长颈漏斗分离出乙酸与乙醇反应的产物 | |
| B. | 用向上排空气法收集铜粉与稀硝酸反应产生的NO | |
| C. | 配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 | |
| D. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 |
7.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A. | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| B. | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
| C. | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D. | 比较水与乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
| A. | A | B. | B | C. | C | D. | D |
6.分子式为C4H8Cl2的有机物共有(不含立体异构)( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
5.常温下,在物质的量浓度之比为3:1的NaCl和H2SO4的混合溶液中,先滴入几滴紫色石蕊试液后,再用铂电极电解该混合溶液.根据电极产物和现象判断,该电解过程可明显分为三个阶段.下列叙述中,不正确的是( )
| A. | 第一阶段中阴、阳两极产生的气体混合引燃后,恰好完全反应得到HCl | |
| B. | 阴极自始至终只产生H2 | |
| C. | 电解过程中,溶液的pH不断增大,最后等于7 | |
| D. | 电解过程中,Na+和SO42-的物质的量保持不变 |
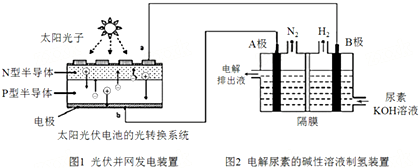
4.氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术.有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气.光伏发电是当今世界利用太阳能最主要方式之一.图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列说法不正确的是( )
0 156254 156262 156268 156272 156278 156280 156284 156290 156292 156298 156304 156308 156310 156314 156320 156322 156328 156332 156334 156338 156340 156344 156346 156348 156349 156350 156352 156353 156354 156356 156358 156362 156364 156368 156370 156374 156380 156382 156388 156392 156394 156398 156404 156410 156412 156418 156422 156424 156430 156434 156440 156448 203614

| A. | 图1中N型半导体为负极 | |
| B. | 若A极产生7.00gN2,则此时B极产生16.8L H2(标况下) | |
| C. | 电解完毕后电解液的pH增大 | |
| D. | 该系统工作时,A极的电极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O |
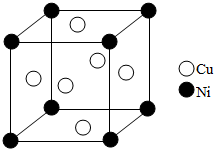 东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题: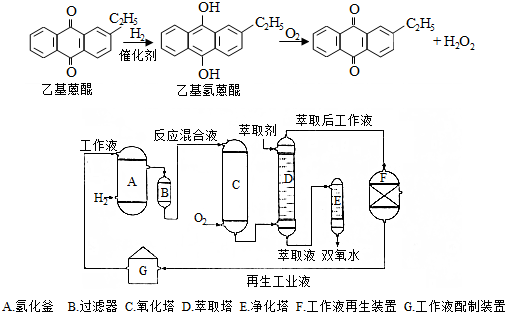
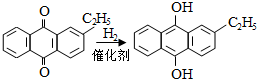 .进入氧化塔C的反应混合液中的主要溶质为乙基氢蒽醌.
.进入氧化塔C的反应混合液中的主要溶质为乙基氢蒽醌.