17.下列实验中,对应的操作,现象以及结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将铜粉加入到浓硫酸中 | 无明显现象 | 铜被浓硫酸钝化 |
| B | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末 | 产生红褐色沉淀 | 除去MgCl2溶液中的Fe3+ |
| C | 将混有乙酸的乙酸乙酯加入到分液漏斗中,加入氢氧化钠溶液,振荡,静置,分液 | 溶液分层 | 除去乙酸乙酯中的乙酸 |
| D | 分别向两只试管中加入同浓度,同体积的草酸溶液,再分别加入同体积、不同浓度的酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色时间不同 | 浓度不同反应速率不同 |
| A. | A | B. | B | C. | C | D. | D |
16.某有机化合物结构简式如图,下列有关说法不正确的是( )


| A. | 该有机化合物分子式为C10H10O3 | |
| B. | 1mol该有机化合物最多可与2molNaOH发生中和反应 | |
| C. | 该有机化合物中两种官能团之间可以发生酯化反应 | |
| D. | 该有机化合物和乙烯均能使酸性高锰酸钾溶液褪色 |
15.化学与生产、生活、社会密切相关,下列说法正确的是( )
| A. | 医用酒精是用淀粉类植物经过发酵后蒸馏制得,浓度通常是75% | |
| B. | 为防止电池中的重金属污染土壤和水体,应将废电池深埋 | |
| C. | “海水淡化”可以解決“淡水供应危机”,向海水中加入明矾可以使海水淡化 | |
| D. | 小苏打是制作面包等糕点的膨松剂.也是胃溃疡病人的治疗药物 |
12.下列四幅谱图是结构简式为CH3CH2OH、CH3OCH3、CH3CH2CH2OH和 的四种有机物的1H核磁共振谱(1H-NMR).其中属于CH3CH2CH2OH的1H-NMR谱图的是( )
的四种有机物的1H核磁共振谱(1H-NMR).其中属于CH3CH2CH2OH的1H-NMR谱图的是( )
 的四种有机物的1H核磁共振谱(1H-NMR).其中属于CH3CH2CH2OH的1H-NMR谱图的是( )
的四种有机物的1H核磁共振谱(1H-NMR).其中属于CH3CH2CH2OH的1H-NMR谱图的是( )| A. |  | B. |  | C. |  | D. |  |
11.下列说法不正确的是( )
0 156235 156243 156249 156253 156259 156261 156265 156271 156273 156279 156285 156289 156291 156295 156301 156303 156309 156313 156315 156319 156321 156325 156327 156329 156330 156331 156333 156334 156335 156337 156339 156343 156345 156349 156351 156355 156361 156363 156369 156373 156375 156379 156385 156391 156393 156399 156403 156405 156411 156415 156421 156429 203614
| A. | 质谱法是快速、微量、精确测定相对分子质量的方法 | |
| B. | 红外光谱仪不可用于测定化合物的官能团 | |
| C. | 用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 氯溴碘代甲烷存在同分异构体 |

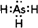 .
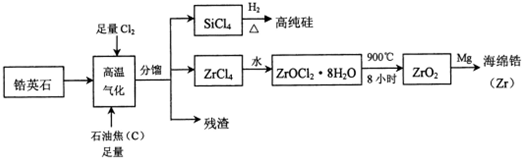
.
 .
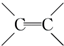
. BHC≡CHCCH2=CH2D
BHC≡CHCCH2=CH2D ECH3CH3.
ECH3CH3. +Br2
+Br2
 .
. $\stackrel{稀,冷KMnO_{4},溶液/OH-}{→}$
$\stackrel{稀,冷KMnO_{4},溶液/OH-}{→}$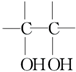 .请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式
.请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式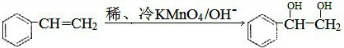 .
. .
. .
.