2.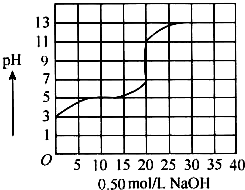 在100mL盐酸的溶液中,以0.50mol/L氢氧化钠溶液滴定后得滴定曲线如图所示,下列叙述正确的是( )
在100mL盐酸的溶液中,以0.50mol/L氢氧化钠溶液滴定后得滴定曲线如图所示,下列叙述正确的是( )
 在100mL盐酸的溶液中,以0.50mol/L氢氧化钠溶液滴定后得滴定曲线如图所示,下列叙述正确的是( )
在100mL盐酸的溶液中,以0.50mol/L氢氧化钠溶液滴定后得滴定曲线如图所示,下列叙述正确的是( )| A. | 盐酸在滴定前的浓度是0.3mol/L | |
| B. | 该盐酸稀释10倍后pH为4 | |
| C. | 滴定过程为求滴定终点,指示剂只能用酚酞 | |
| D. | 若用酚酞作指示剂,滴定终点时溶液颜色的变化为红色到无色 |
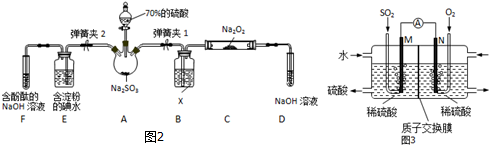
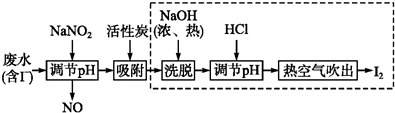
20.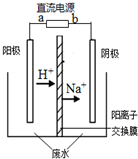 最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )
最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )
 最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )
最近有研究人员利用隔膜电解法处理高浓度的乙醛废水.乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸.实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法不正确的是( )| A. | 电解过程中,阳极附近的乙醛被氧化 | |
| B. | 阳极反应CH3CHO-2e-+H2O═CH3COOH+2H+ | |
| C. | 若以CH4-空气燃料电池为直流电源,燃料电池的b极应通入CH4 | |
| D. | 现处理含1mol乙醛的废水,至少需转移2mol电子 |
18.甲醇是21世纪应用最广泛的清洁燃料之一,也是农药、医药的重要原料.请回答下列问题:
(1)已知,CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.5kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
则如图1表示工业上以CO2(g)、H2(g)为原料合成该甲醇反应的能量变化示意图中正确的是a(填字母代号).
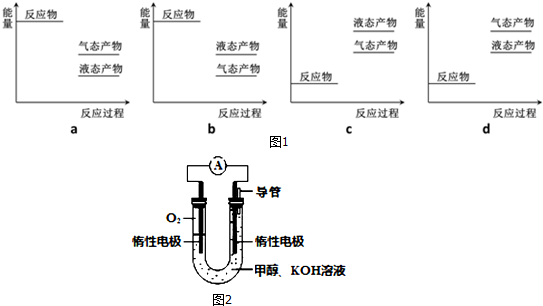
(2)CO和H2反应也能合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.1kJ•mol-1.在250℃下,将一定量的CO和H2投入10L的恒容密闭容器中,各物质的浓度(mol•L-1)变化如下表所示(前6min没有改变条件):
①x=0.14.
②若6~8min时只改变了一个条件,则改变的条件是充入一定量H2,第8min时,该反应是否达到平衡状态?不是(填“是”或“不是”).
③若容器容积不变,下列措施可增加甲醇产率的是BD(填序号).
A.升高温度
B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大
D.再充入1mol CO和3mol H2
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
①该电池负极的电极反应为CH3OH-6e-+8OH-=CO32-+6H2O;
②该电池工作时,溶液中的OH-向负极移动.
(1)已知,CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.5kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
则如图1表示工业上以CO2(g)、H2(g)为原料合成该甲醇反应的能量变化示意图中正确的是a(填字母代号).

(2)CO和H2反应也能合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.1kJ•mol-1.在250℃下,将一定量的CO和H2投入10L的恒容密闭容器中,各物质的浓度(mol•L-1)变化如下表所示(前6min没有改变条件):
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
②若6~8min时只改变了一个条件,则改变的条件是充入一定量H2,第8min时,该反应是否达到平衡状态?不是(填“是”或“不是”).
③若容器容积不变,下列措施可增加甲醇产率的是BD(填序号).
A.升高温度
B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大
D.再充入1mol CO和3mol H2
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
①该电池负极的电极反应为CH3OH-6e-+8OH-=CO32-+6H2O;
②该电池工作时,溶液中的OH-向负极移动.
17.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 200 g 63%的浓硝酸中含氧原子个数为6NA | |
| B. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的数目大于6NA |
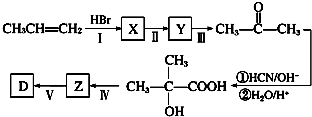
15.合成具有美白作用的化妆品原料Z的反应原理如下:
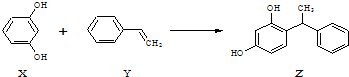
下列叙述不正确的是( )

下列叙述不正确的是( )
| A. | X、Z均能与Na2CO3溶液反应 | |
| B. | X可作缩聚反应单体,Y可作加聚反应单体 | |
| C. | X、Y、Z均能使溴水褪色,但是原理不相同 | |
| D. | 该反应的反应类型为取代反应 |
13.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
0 156231 156239 156245 156249 156255 156257 156261 156267 156269 156275 156281 156285 156287 156291 156297 156299 156305 156309 156311 156315 156317 156321 156323 156325 156326 156327 156329 156330 156331 156333 156335 156339 156341 156345 156347 156351 156357 156359 156365 156369 156371 156375 156381 156387 156389 156395 156399 156401 156407 156411 156417 156425 203614
| A. | 室温下向1 L pH=1的醋酸溶液中加水,所得溶液的OH-数目大于0.1NA | |
| B. | 60g乙酸与足量乙醇发生酯化反应,充分反应后乙酸断裂的C-O键数目为NA | |
| C. | 已知C2H4(g)+H2(g)=C2H6(g)△H=-137.0 kI/mol,乙烯与H2加成时放出68.5 kJ热量,则 反应过程中被破坏的碳原子之间共用电子对数目为NA | |
| D. | 4.6gSO2、NO2混合气体中含有中子数为2.3 NA |
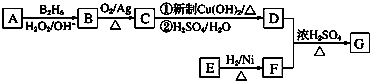
 .
.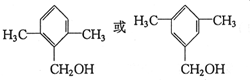 (任意填一种).
(任意填一种).