12.下列有关 Na2SO3溶液的叙述不正确的是( )
| A. | 该溶液中,K+、CO32-、Br-、ClO-能大量共存 | |
| B. | 不能用稀硝酸酸化的硝酸钡溶液检验该溶液是否变质 | |
| C. | 将此溶液与稀硫酸产生的少量气体通入足量的NaAlO2溶液中制Al(OH)3:2AlO2-+SO2+3H2O═2Al(OH)3↓+SO32- | |
| D. | 能使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O |
10.关于明矾KAl(SO4)2•12H2O溶液,下列说法正确的是( )
| A. | 向该溶液中加入过量NaOH溶液,仍能大量存在:ClO-、K+、CO32-、Cl- | |
| B. | 用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+ | |
| C. | 向该溶液中加入过量Ba(OH)2溶液,有白色沉淀生成2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 将该溶液蒸干、灼烧得到是K 2SO4和Al2O3 |
9.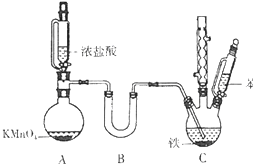 氯苯是重要的有机化工原料.实验室制备氯苯的反应原理、实验装置如图所示(加热装置已略去):
氯苯是重要的有机化工原料.实验室制备氯苯的反应原理、实验装置如图所示(加热装置已略去):
可能用到的有关数据如下: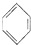 +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$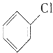 +HCl
+HCl
在装置A中利用浓盐酸和KMnO4反应缓慢制备氯气,把氯气干燥后通入装有39mL苯的反应器C中(内有铁屑作催化剂),维持反应温度在40~60℃,回流40分钟.温度过高会产生过多的邻二氯苯和对二氯苯.反应结束后,冷却至室温.将C中的液体倒入分液漏斗中,分别用NaOH溶液和蒸馏水洗涤,分离出的产物干燥后,进行蒸馏纯化,得到22g纯净的氯苯.
回答下列问题:
(1)A装置中制备氯气的离子方程式为2MnO4-+16H++10Cl-=2Mn2+↑+5C12↑+8H2O.
(2)B装置中盛放的药品为CaCl2或P2O5,C装置中采用的加热方法最好为40℃-60℃的水浴加热.
(3)已知浓盐酸和苯都具有较强的挥发性.采用如图所示装置加入液体的优点是防止液体挥发,能够平衡压强,使液体顺利流下.
(4)用氢氧化钠溶液洗涤可以除去杂质的化学式为HCl、Cl2、FeCl3,检验产品洗涤干净的方法为取最后一次洗涤液于试管中,加入硝酸银,若不出现沉淀,则证明已经洗干净.
(5)该实验存在一定缺陷,改进措施为将冷凝管上端逸出的HCl、Cl2通入NaOH溶液中,防止污染空气.
(6)该实验所得氯苯的产率为44.4%(保留小数点后一位).
 氯苯是重要的有机化工原料.实验室制备氯苯的反应原理、实验装置如图所示(加热装置已略去):
氯苯是重要的有机化工原料.实验室制备氯苯的反应原理、实验装置如图所示(加热装置已略去):可能用到的有关数据如下:
 +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl
+HCl| 沸点(℃) | 密度(g•mL-1) | 溶解性 | |
| 苯 | 80.1 | 0.88 | 难溶于水 |
| 氯苯 | 132.2 | 1.10 | 难溶于水,易溶于有机溶剂 |
| 对二氯苯 | 173.4 | 1.46 | 难溶于水,易溶于有机溶剂 |
| 邻二氯苯 | 180.4 | 1.30 | 难溶于水,易溶于有机溶剂 |
回答下列问题:
(1)A装置中制备氯气的离子方程式为2MnO4-+16H++10Cl-=2Mn2+↑+5C12↑+8H2O.
(2)B装置中盛放的药品为CaCl2或P2O5,C装置中采用的加热方法最好为40℃-60℃的水浴加热.
(3)已知浓盐酸和苯都具有较强的挥发性.采用如图所示装置加入液体的优点是防止液体挥发,能够平衡压强,使液体顺利流下.
(4)用氢氧化钠溶液洗涤可以除去杂质的化学式为HCl、Cl2、FeCl3,检验产品洗涤干净的方法为取最后一次洗涤液于试管中,加入硝酸银,若不出现沉淀,则证明已经洗干净.
(5)该实验存在一定缺陷,改进措施为将冷凝管上端逸出的HCl、Cl2通入NaOH溶液中,防止污染空气.
(6)该实验所得氯苯的产率为44.4%(保留小数点后一位).
8.下列各选项有机物数目,与分子式为ClC4H7O2 且能与碳酸氢钠反应生成气体的有机物数目相同的是(不含立体异构)( )
| A. | 分子式为C5H10 的烯烃 | B. | 分子式为C4H8O2的酯 | ||
| C. | 甲苯( 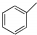 )的一氯代物 )的一氯代物 | D. | 立体烷 (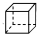 )的二氯代物 )的二氯代物 |
7.向0.1mol/L的NH4HCO3溶液中逐滴加入0.1mol/LNaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量分数).根据图象,下列说法不正确的是( )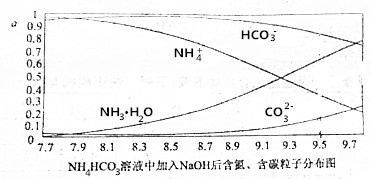

| A. | 开始阶段,HCO3-反而略有增加,可能是因为NH4HCO3溶液中存在H2CO3发生的主要反应是H2CO3+OH-═HCO3-+H2O | |
| B. | 当pH大于8.7以后,碳酸氢根离子和铵根离子同时与氢氧根离子反应 | |
| C. | pH=9.5时,溶液中c(HCO3-)>c(HN3•H2O)>c(NH4+)>c(CO32-) | |
| D. | 滴加氢氧化钠溶液时,首先发生的反应为2NH4HCO3+2NaOH═(NH4)2CO3+Na2CO3 |
6.以下说理不严谨的是( )
| A. | 二氯甲烷只有一种,说明甲烷分子是立体结构 | |
| B. | 2-丁烯四个碳原子共平面,说明乙烯分子是平面结构 | |
| C. | 苯乙炔分子中所有原子共平面,说明乙炔分子中原子在一条直线上 | |
| D. | 邻二甲苯只有一种,说明苯分子中不存在单双键交替的碳碳键. |
4.短周期主族元素X、Y、Z、W的原子序数均为偶数且依次增大,元素X原子的最外层电子数是其内层电子总数的3倍,下列说法错误的是( )
| A. | 元素X的简单气态氢化物的热稳定性比W的强 | |
| B. | 元素W的最高价氧化物对应水化物的酸性比Z的强 | |
| C. | 元素Y、Z的单质都有金属光泽 | |
| D. | X分别与Y、Z、W形成的化合物所含化学键类型相同 |
3.NA为阿伏伽德罗常数,下列说法错误的是( )
0 156224 156232 156238 156242 156248 156250 156254 156260 156262 156268 156274 156278 156280 156284 156290 156292 156298 156302 156304 156308 156310 156314 156316 156318 156319 156320 156322 156323 156324 156326 156328 156332 156334 156338 156340 156344 156350 156352 156358 156362 156364 156368 156374 156380 156382 156388 156392 156394 156400 156404 156410 156418 203614
| A. | 1molNa与O2反应得到32g固体产物,钠失去电子数为NA | |
| B. | 用1mL0.1mol•L-1FeCl3溶液制得的氢氧化铁胶体所含胶粒数为10-4NA | |
| C. | 12g金刚石中含有的共价键数为2NA | |
| D. | 标准状况下,22.4LCH4中含有的碳原子数为NA |
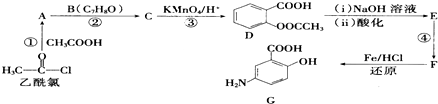
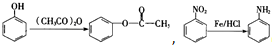 ,(具有还原性,极易被氧化)
,(具有还原性,极易被氧化) .
. .
.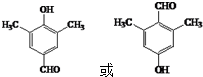 (写出其中一种结构简式).
(写出其中一种结构简式).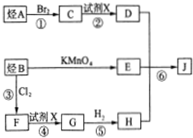
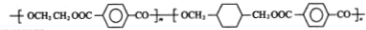
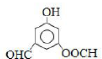 .
.