2.填写如表
(1)
(2)画出下列粒子的结构示意图:S2-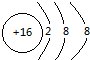 Mg2+
Mg2+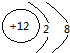 .
.
(1)
| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 | |
| ① | ${\;}_{19}^{40}$K | 19 | 21 | 19 | 40 |
| ② | 3818Ar | 18 | 20 | 18 | 38 |
| ③ | 3216S2- | 16 | 16 | 18 | 32 |
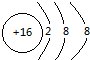 Mg2+
Mg2+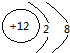 .
.
1.化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如果设法提高化学反应的限度,下面说法错误的是( )
| A. | 能够节约原料和能源 | B. | 能提高产品的产量 | ||
| C. | 能够提高化学反应速率 | D. | 能够提高经济效益 |
3.X、Y、Z、R、W均为前四周期的主族元素,其位置关系如图所示.下列说法正确的是( )
| X | |||
| Y | Z | R | |
| W |
| A. | 五种元素的原子最外层电子数一定大于2 | |
| B. | 五种元素一定都是非金属元素 | |
| C. | R 的最高价氧化物对应的水化物一定是强酸 | |
| D. | X的氢化物沸点一定比Z的氢化物沸点高 |
1.要除去乙酸乙酯中少量的乙酸,下列实验方案正确的是( )
| A. | 在混合液中加入氢氧化钠溶液,充分振荡后分液 | |
| B. | 在混合液中加人一定量的浓硫酸和乙醇,加热,将乙酸转化为乙酸乙酯 | |
| C. | 在混合液中加人足量的水.充分振荡后分液 | |
| D. | 在混合液中加入适量的饱和碳酸钠溶液,充分振荡后分液 |
20.下列说法正确的是( )
| A. | 石油的裂化、煤的液化、蛋白质的盐析、焰色反应都是化学变化 | |
| B. | 在元素周期表的金属和非金属分界线附近可寻找锗、硅、硒等半导体材料 | |
| C. | 铅蓄电池是常见的二次电池.性能优良.比能量高.缺点是废弃电池污染严重 | |
| D. | 在新型催化剂条件下通过电力可将二氧化碳氧化为甲醇、甲烷等燃料 |
17.X和Y均为短周期元素,已知aXn-比bYm+多两个电子层,下列说法正确的是( )
| A. | b<2 | B. | X只能位于第三周期 | ||
| C. | a+n-b+m=10或16 | D. | Y不可能位于第二周期 |
16.X、Y、Z、W、Q五种短周期主族元素的原子序数依次增大,它们的原子最外层电子数之和为18,X和Z同主族,且单质在常温下状态不同,W形成的简单离子在同周期元素形成的简单离子中半径是最小的,而Q的原子半径在同周期元素中最小,则下列说法正确的是( )
0 156219 156227 156233 156237 156243 156245 156249 156255 156257 156263 156269 156273 156275 156279 156285 156287 156293 156297 156299 156303 156305 156309 156311 156313 156314 156315 156317 156318 156319 156321 156323 156327 156329 156333 156335 156339 156345 156347 156353 156357 156359 156363 156369 156375 156377 156383 156387 156389 156395 156399 156405 156413 203614
| A. | X、Y两种元素形成的化合物中原子个数比一定为2:1 | |
| B. | Z、Y两种元素形成的化合物中只能含有离子键 | |
| C. | W元素形成的单质熔点很高,是一种优良的耐火材料 | |
| D. | Z、W、Q三种元素的最高价氧化物对应的水化物能两两反应 |
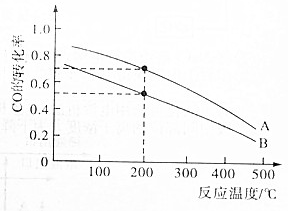 高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题.
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题.