5.下列分子或离子中,中心原子含有孤对电子的是( )
| A. | NH4+ | B. | CCl4 | C. | SiH4 | D. | PH3 |
1.下表是元素周期表的一部分,用元素符号或化学式回答下列问题:
(1)最高价氧化物对应的水化物中酸性最强的酸的化学式HClO4,该酸与NaOH溶液反应的离子方程式是:H++OH-=H2O
(2)写出有序号标出的元素中金属性最强的元素在元素周期表中的位置第三周期IA族.
(3)标况下,1mol的①在④中完全燃烧放出285.8kJ热量,写出该反应的热化学方程式2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol.
(4)写出从两种不同角度比较⑥与⑦两种元素金属性的方法根据金属与水或酸反应剧烈程度,比较最高价氧化物对应水化物的碱性强弱.
| 周期 族 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)写出有序号标出的元素中金属性最强的元素在元素周期表中的位置第三周期IA族.
(3)标况下,1mol的①在④中完全燃烧放出285.8kJ热量,写出该反应的热化学方程式2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol.
(4)写出从两种不同角度比较⑥与⑦两种元素金属性的方法根据金属与水或酸反应剧烈程度,比较最高价氧化物对应水化物的碱性强弱.
20.下表为六种短周期元素的部分性质,下列有关说法错误的是( )
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.66 | 0.70 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A. | X与Y可以形成阴离子XY32- | |
| B. | 元素R的氧化物对应水化物一定为强酸 | |
| C. | Y2-的半径要小于R- | |
| D. | 由X形成的化合物QX和XR4,其晶体类型不相同 |
19.对于反应A(g)+3B(g)??2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
( )
( )
| A. | v(A)=0.5mol•(L•min)-1 | B. | v(B)=0.4mol•(L•s)-1 | ||
| C. | v(B)=0.3mol•(L•s)-1 | D. | v(C)=0.2mol•(L•s)-1 |
18.下列各组物质的性质比较中不正确的是( )
0 156192 156200 156206 156210 156216 156218 156222 156228 156230 156236 156242 156246 156248 156252 156258 156260 156266 156270 156272 156276 156278 156282 156284 156286 156287 156288 156290 156291 156292 156294 156296 156300 156302 156306 156308 156312 156318 156320 156326 156330 156332 156336 156342 156348 156350 156356 156360 156362 156368 156372 156378 156386 203614
| A. | 氧化性:F2>C12>Br2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 熔沸点:SiO2>NaCl>CO2 | D. | 热稳定性:SiH4>PH3>H2S |
 现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答: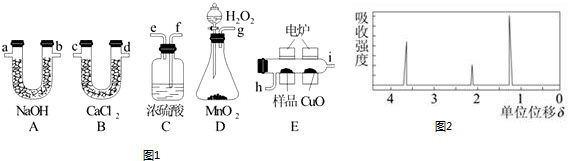
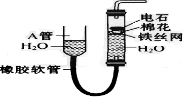 如图中的实验装置可用于制取乙炔. 请填空:
如图中的实验装置可用于制取乙炔. 请填空: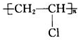 .
.