5.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下表所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 四种元素的单质中,Z单质的熔沸点最高 | |
| D. | X的单质能与H2反应,生成一种弱酸性的物质 |
4.某元素Z的核外电子数等于核内中子数,取其单质2.8g 与O2完全反应,可得6g化合物ZO2,Z 元素在周期表中位置是( )
①第3周期 ②第2周期 ③第ⅣA 族 ④第ⅤA族.
①第3周期 ②第2周期 ③第ⅣA 族 ④第ⅤA族.
| A. | ②④ | B. | ①④ | C. | ①③ | D. | ②③ |
3.元素的性质随原子序数的递增呈周期性变化的原因是( )
| A. | 元素原子的电子层数呈周期性变化 | |
| B. | 元素原子的核外电子排布呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素原子半径呈周期性变化 |
2.下列关于物质结构的说法中正确的是( )
| A. | BF3、HClO分子中所有原子都满足最外层8电子结构 | |
| B. | 某元素原子最外层电子数是次外层电子数的a(a为整数)倍,则该原子核内质子数为2a+2 | |
| C. | D2O分子与H2O分子是所含电子总数不相等的分子 | |
| D. | 在任何物质分子中都含有化学键 |
1.下列操作正确的是( )
| A. | 锥形瓶在装待测液前要用待测液润洗2~3次 | |
| B. | 用25mL酸式滴定管量取20.00mLKMnO4溶液 | |
| C. | 测某溶液pH:用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测 | |
| D. | 加热蒸发NaHCO3溶液得纯净的NaHCO3 |
20.A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层电子数是最外层电子数的2倍,则A、B元素 ( )
| A. | 一定是第2周期元素 | B. | 一定是同一主族元素 | ||
| C. | 可能是第2、3周期元素 | D. | 可以相互化合形成化合物 |
19.与氢氧根具有相同的质子数和电子数的微粒是( )
| A. | CH4 | B. | NH4 + | C. | NH2- | D. | Cl- |
18.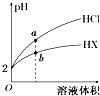 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | a、b两点:c(X-)>c(Cl-) | B. | 稀释10倍,HX溶液的pH=3 | ||
| C. | 稀释前,c(HX)=0.01 mol•L-1 | D. | 溶液的导电性:a>b |
17.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放.下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥酯化反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥酯化反应.
| A. | ①④ | B. | ②③ | C. | ⑤⑥ | D. | ②⑤ |
16.下列离子方程式正确的是( )
0 156182 156190 156196 156200 156206 156208 156212 156218 156220 156226 156232 156236 156238 156242 156248 156250 156256 156260 156262 156266 156268 156272 156274 156276 156277 156278 156280 156281 156282 156284 156286 156290 156292 156296 156298 156302 156308 156310 156316 156320 156322 156326 156332 156338 156340 156346 156350 156352 156358 156362 156368 156376 203614
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 金属钾与水反应:2K+2H2O═2K++2OH-+H2↑ | |
| C. | 铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ | |
| D. | 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O |