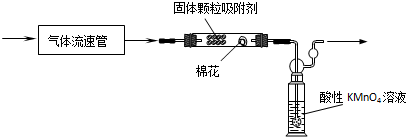
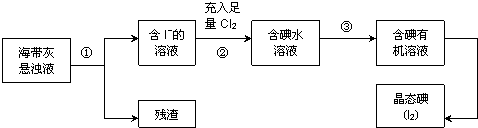
14.下列说法错误的是( )
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、H+和H2是氢元素的四种不同粒子 | |
| B. | ${\;}_{20}^{40}$Ca和 ${\;}_{20}^{42}$Ca、石墨和金刚石均为同位素 | |
| C. | ${\;}_{1}^{1}$H和 ${\;}_{1}^{2}$H是不同的核素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
13.下列说法错误的是( )
| A. | 只用水可以鉴别甲苯和四氯化碳 | |
| B. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| C. | 乙醇分子中不含有OH- | |
| D. | 95%的乙醇溶液常用于医疗消毒 |
12.在通常情况下,下列各组物质的性质排列不正确的是( )
| A. | 沸点:己烷>2-甲基丁烷>戊烷 | B. | 同分异构体种类:戊烷<戊烯 | ||
| C. | 密度:苯<水<1,1,2,2-四溴乙烷 | D. | 点燃时火焰明亮程度:乙烯>乙烷 |
11.下列各有机物中,属于烃的是( )
| A. | 氯丁烷 | B. | 苯的同系物 | C. | 硝基苯 | D. | 乙醇 |
7.下列物质中均既有离子键又有共价键的一组是( )
0 156177 156185 156191 156195 156201 156203 156207 156213 156215 156221 156227 156231 156233 156237 156243 156245 156251 156255 156257 156261 156263 156267 156269 156271 156272 156273 156275 156276 156277 156279 156281 156285 156287 156291 156293 156297 156303 156305 156311 156315 156317 156321 156327 156333 156335 156341 156345 156347 156353 156357 156363 156371 203614
| A. | NaOH、H2O、NH4Cl | B. | KOH、Na2O2、NH4Cl | ||
| C. | MgO、CaBr2、NaCl | D. | Na2SO4、HCl、MgCl2 |
 .
.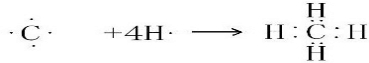 .
.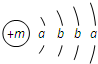 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.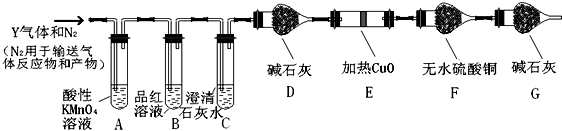 (2)写出产生CO2的化学方程式C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.
(2)写出产生CO2的化学方程式C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.