10.下列属于人工合成的高分子化合物是( )
| A. | 聚氯乙烯 | B. | 淀粉 | C. | 乙酸乙酯 | D. | 苯乙烯 |
9.在含有Na+、Cl-、CO32-离子的溶液中,能大量共存的离子是( )
| A. | K+ | B. | H+ | C. | Ca2+ | D. | Ag+ |
8.下列有关如图所示原电池装置描述正确的是( )
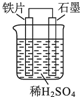

| A. | 石墨电极作负极 | |
| B. | 铁片上的反应:Fe-2e-=Fe2+ | |
| C. | 铁电极附近溶液中氢离子浓度增大 | |
| D. | 电子由石墨电极通过导线流向铁电极 |
7.在钠与水反应的实验操作中,符合化学实验安全规则的是( )
| A. | 不经切割,直接用大块的钠做实验 | B. | 用手小心抓住钠块投入烧杯中 | ||
| C. | 在烧杯口盖上玻片后再观察现象 | D. | 将剩余的钠块放入废液缸 |
6.在萃取-分液实验中,振荡分液漏斗的操作正确的是( )
| A. |  | B. | 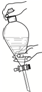 | C. |  | D. | 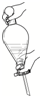 |
5.下列能正确表示Mg的原子结构示意图的是( )
| A. |  | B. | 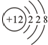 | C. |  | D. |  |
4.下表为元素周期表的一部分,请回答有关问题
(1)⑤和⑧的元素符号是Si和Ar.
(2)表中最活泼的金属元素是钾,形成化合物种类最多的元素是碳(填写元素名称).
(3)表中能形成两性氢氧化物的元素是Al,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O;Al(OH)3+KOH=KAlO2+2H2O.
(4)证明元素⑥、⑦非金属性强弱,用一个化学方程式表示:Cl2+Na2S═2NaCl+S↓.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属元素是钾,形成化合物种类最多的元素是碳(填写元素名称).
(3)表中能形成两性氢氧化物的元素是Al,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O;Al(OH)3+KOH=KAlO2+2H2O.
(4)证明元素⑥、⑦非金属性强弱,用一个化学方程式表示:Cl2+Na2S═2NaCl+S↓.
1.X、Y、Z、R、M是元素周期表中原子序数依次增大的五种短周期元素,其相关信息如下表:
(1)Y、Z、R的第一电离能从大到小的顺序是N>O>C(填元素符号)
(2)Z、R的最简单氢化物中稳定性强的是H2O,沸点高的是H2O(填化学式)
(3)甲是由上述3种元素组成的常见化合物,常温下pH=3的甲溶液中由水电离c(H+)=10-3mol/L,则甲的化学式是NH4NO3.
(4)直线型分子Y2Z2中所有原子都达到8电子稳定结构,则分子中σ键与π键的个数之比是3:4.
(5)常温下0.58gY4H10完全燃烧放出29kJ的热量,请写出Y4H10燃烧热的热化学方程式C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol.
0 156154 156162 156168 156172 156178 156180 156184 156190 156192 156198 156204 156208 156210 156214 156220 156222 156228 156232 156234 156238 156240 156244 156246 156248 156249 156250 156252 156253 156254 156256 156258 156262 156264 156268 156270 156274 156280 156282 156288 156292 156294 156298 156304 156310 156312 156318 156322 156324 156330 156334 156340 156348 203614
| 元素 | 相关信息 |
| X | X的一种核素的原子核中没有中子 |
| Y | Y原子的核外电子占据4个原子轨道 |
| Z | Z的气态氢化物能使湿润的红色石蕊试纸变蓝 |
| R | R是地壳中含量最高的元素 |
| M | M的单质与冷水剧烈反应,生成的强碱中含有电子数相同的阴阳离子 |
(2)Z、R的最简单氢化物中稳定性强的是H2O,沸点高的是H2O(填化学式)
(3)甲是由上述3种元素组成的常见化合物,常温下pH=3的甲溶液中由水电离c(H+)=10-3mol/L,则甲的化学式是NH4NO3.
(4)直线型分子Y2Z2中所有原子都达到8电子稳定结构,则分子中σ键与π键的个数之比是3:4.
(5)常温下0.58gY4H10完全燃烧放出29kJ的热量,请写出Y4H10燃烧热的热化学方程式C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol.
 ,碳氢键之间键角为109°28′.甲烷和氯气在光照下发生取代反应,生成5种产物.产物中CCl4常用作灭火剂.试写出三溴甲烷在光照条件下与溴蒸气反应的化学方程式:CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr.
,碳氢键之间键角为109°28′.甲烷和氯气在光照下发生取代反应,生成5种产物.产物中CCl4常用作灭火剂.试写出三溴甲烷在光照条件下与溴蒸气反应的化学方程式:CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr.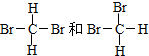 (在横线上填相应的序号)
(在横线上填相应的序号)