20.近年来,我国在超导体材料研究方面居于世界领先地位,铊(Tl)是超导体的组成成分之一,铊位于第6周期ⅢA族.下列对铊的性质的推导不正确的是( )
| A. | 是易导电的银白色金属 | B. | Tl(OH)3是两性氢氧化物 | ||
| C. | Tl3+能形成+3价的化合物 | D. | 单质能与稀硝酸反应生成硝酸盐 |
19.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是( )
| A. | NH4+、CO32-、K+、Na+ | B. | Na+、Ba2+、Cl-、HCO3- | ||
| C. | NO3-、Cu2+、K+、SO42- | D. | K+,Na+,Cl-,NO3- |
18.A+、B2+、C-、D2- 四种离子核外电子排布相同,则这四种离子半径大小顺序是( )
| A. | C->D2->A+>B2+ | B. | B2+>A+>C->D2- | C. | B2+>A+>D2->C- | D. | D2->C->A+>B2+ |
16.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的硫酸和锌反应的实验数据,下列有关叙述正确的是( )
| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的状态 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m2 |
| 3 | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
| 4 | 50.0 | 6.0 | 粉末 | 25 | t2 | 14.9 |
| 5 | 50.0 | 8.0 | 粉末 | 25 | t3 | 19.3 |
| 6 | 50.0 | 10.0 | 粉末 | 25 | t4 | m3 |
| A. | t1>70 | |
| B. | m3=19.3 | |
| C. | 实验1、实验2与实验3探究的是温度对化学反应速率的影响 | |
| D. | 无法计算出硫酸的物质的量浓度 |
13.下列说法中,正确的是( )
| A. | 卤代烃在NaOH的醇溶液中共热均能发生消去反应生成烯烃 | |
| B. | 凡是能发生银镜反应的物质都属于醛类 | |
| C. | 能与FeCl3溶液作用显紫色的有机物一般含有酚羟基 | |
| D. | 酯类水解均能生成含相同碳原子数的羧酸和醇 |
12. 硫酸工业生产应考虑综合经济效益问题.
硫酸工业生产应考虑综合经济效益问题.
(1)若从下列四个城市中选择一处建一座硫酸厂,你认为厂址宜选在C的郊区(填标号).
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)CuFeS2是黄铁矿的另一成分,煅烧时CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为4CuFeS2+13O2=4CuO+2Fe2O3+8SO2;
(3)为了有利于SO2转化SO3,多采用如图所示的装有多层催化剂的接触室(填设备名称)作为反应设备,让气体经历如图所示流程而不是直接进入该设备进行反应的原因是使热量能充分利用.
(4)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都是正确的是D
A.黄铁矿燃烧前需要粉碎,因为大块的黄铁矿不能在空气中 燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中的二氧化硫会与杂质反应
C.二氧化硫氧化为三氧化硫时需使用催化剂,这样可以提高二氧化硫的转化率
D.三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率
(5)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据如表信息,结合工业生产实际,选择最合适的生产条件是400℃、1个大气压.
(6)由吸收塔排出的尾气中SO2的含量超过500umol/L,就要用氨水洗涤烟气脱硫,该反应的化学方程式为2NH3•H2O+SO2=(NH4)2SO3+H2O.
(7)若用浓硫酸吸收SO3可以得到H2SO4•SO3.用1000g 98% 的H2SO4充分吸收SO3后,再进行稀释,可以得到98% 的硫酸的质量是C
A.1.98kg B.2.00kg C.2.22kg D.2.42kg.
0 156149 156157 156163 156167 156173 156175 156179 156185 156187 156193 156199 156203 156205 156209 156215 156217 156223 156227 156229 156233 156235 156239 156241 156243 156244 156245 156247 156248 156249 156251 156253 156257 156259 156263 156265 156269 156275 156277 156283 156287 156289 156293 156299 156305 156307 156313 156317 156319 156325 156329 156335 156343 203614
 硫酸工业生产应考虑综合经济效益问题.
硫酸工业生产应考虑综合经济效益问题.(1)若从下列四个城市中选择一处建一座硫酸厂,你认为厂址宜选在C的郊区(填标号).
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)CuFeS2是黄铁矿的另一成分,煅烧时CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为4CuFeS2+13O2=4CuO+2Fe2O3+8SO2;
(3)为了有利于SO2转化SO3,多采用如图所示的装有多层催化剂的接触室(填设备名称)作为反应设备,让气体经历如图所示流程而不是直接进入该设备进行反应的原因是使热量能充分利用.
(4)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都是正确的是D
A.黄铁矿燃烧前需要粉碎,因为大块的黄铁矿不能在空气中 燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中的二氧化硫会与杂质反应
C.二氧化硫氧化为三氧化硫时需使用催化剂,这样可以提高二氧化硫的转化率
D.三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率
(5)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据如表信息,结合工业生产实际,选择最合适的生产条件是400℃、1个大气压.
| 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 | |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
(7)若用浓硫酸吸收SO3可以得到H2SO4•SO3.用1000g 98% 的H2SO4充分吸收SO3后,再进行稀释,可以得到98% 的硫酸的质量是C
A.1.98kg B.2.00kg C.2.22kg D.2.42kg.
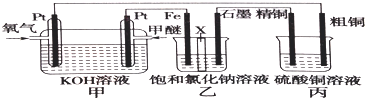
 .
.
 .
.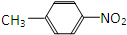 和
和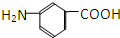 E.35Cl和37Cl
E.35Cl和37Cl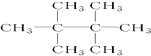 ,
,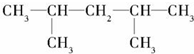 ,该烯烃可能的结构简式有2种.
,该烯烃可能的结构简式有2种.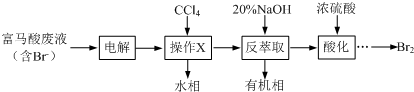
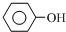 +3Br2→
+3Br2→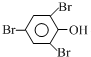 ↓+3HBr
↓+3HBr