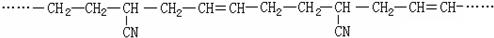9.某研究小组采用矿浆电解法从复杂锑铅矿(主要成分为Sb2S3、PbS、FeS)提取金属锑,实现了锑、铅的一步分离.其工艺流程图如下:

已知:①Sb3++6Cl??SbCl63?
②
(1)加入NH4Cl可以提高电解时SbCl3在阳极区的溶解度,理由是提高氯离子浓度,使Sb3++6Cl-?SbCl63-正向移动.
(2)Sb2S3在阳极区因硫元素被氧化而溶解,写出电极反应式Sb2S3+12Cl--6e-=3S+2SbCl63-或Sb2S3-6e-=3S+2Sb3+; Sb2S3也可以被电解生成的Fe3+溶解,反应的离子方程式为6Fe3++Sb2S3+12Cl-=6Fe2++3S+2SbCl63-或6Fe3++Sb2S3=3S+2Sb3++6Fe2+.
(3)阳极渣中含铅化合物的化学式为PbCl2.
(4)步骤Ⅱ反应选择在40~50℃进行,温度不宜过高的原因是防止NH4HCO3分解.
(5)单质硫在煤油中的溶解度曲线如图2.利用煤油为溶剂将滤渣中的碳酸铅和单质硫分离,步骤Ⅲ的操作方法是:用热煤油溶解,趁热过滤;将滤液冷却,过滤.
(6)步骤Ⅳ,先加入NaClO3试剂将Fe2+转化为Fe2O3•nH2O除去,则氧化剂和还原剂的物质的量之比为1:6.

已知:①Sb3++6Cl??SbCl63?
②
| 物质 | Sb2S3 | PbS | FeS | PbCl2 | PbCO3 |
| Ksp | 2×10?93 | 1×10?28 | 6×10?18 | 1.6×10?5 | 7.4×10?14 |
(2)Sb2S3在阳极区因硫元素被氧化而溶解,写出电极反应式Sb2S3+12Cl--6e-=3S+2SbCl63-或Sb2S3-6e-=3S+2Sb3+; Sb2S3也可以被电解生成的Fe3+溶解,反应的离子方程式为6Fe3++Sb2S3+12Cl-=6Fe2++3S+2SbCl63-或6Fe3++Sb2S3=3S+2Sb3++6Fe2+.
(3)阳极渣中含铅化合物的化学式为PbCl2.
(4)步骤Ⅱ反应选择在40~50℃进行,温度不宜过高的原因是防止NH4HCO3分解.
(5)单质硫在煤油中的溶解度曲线如图2.利用煤油为溶剂将滤渣中的碳酸铅和单质硫分离,步骤Ⅲ的操作方法是:用热煤油溶解,趁热过滤;将滤液冷却,过滤.
(6)步骤Ⅳ,先加入NaClO3试剂将Fe2+转化为Fe2O3•nH2O除去,则氧化剂和还原剂的物质的量之比为1:6.
8.A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,其相关信息如下:
请回答下列问题:
(1)F位于元素周期表第IB族,其简化电子排布式为[Ar]3d104s1 .
(2)D元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断E基态原子的核外电子排布图为: ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.
(4)A与D形成的D2A4分子中D原子的杂化类型为sp3杂化,A与D形成的最简单分子易溶于水的原因氨气分子能与水分子形成氢键.
(5)C的一种单质相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环(如图1).则1个这种单质分子中所含π键的数目为30.
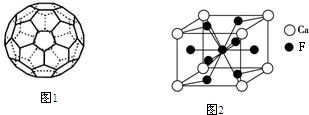
(6)已知在元素周期表中存在“对角线规则”,即周期表中左上方与右下方元素它们的单质及其化合物的性质相似,如Li和Mg,试写出向BeCl2溶液中加入过量的NaOH溶液反应的化学方程式:BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O.
(7)图2是金属Ca和F所形成的某种合金的晶胞结构示意图,已知镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力.已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=5(填数值);氢在合金中的密度为0.083g•cm-3.
| 相关信息 | |
| A | 所处的周期数、族序数分别与其原子序数相等 |
| B | 原子核外电子有4种不同的运动状态 |
| C | 元素原子的核外成对电子数是未成对电子数的2倍且有3个能级 |
| D | 元素原子的核外p电子数比s电子数少1 |
| E | E原子的第一至第四电离能如下:I1=738 kJ•mol-1 I2=1451 kJ•mol-1 I3=7733 kJ•mol-1 I4=10540 kJ•mol-1 |
| F | 第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满 |
(1)F位于元素周期表第IB族,其简化电子排布式为[Ar]3d104s1 .
(2)D元素基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断E基态原子的核外电子排布图为:
 ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.(4)A与D形成的D2A4分子中D原子的杂化类型为sp3杂化,A与D形成的最简单分子易溶于水的原因氨气分子能与水分子形成氢键.
(5)C的一种单质相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环(如图1).则1个这种单质分子中所含π键的数目为30.

(6)已知在元素周期表中存在“对角线规则”,即周期表中左上方与右下方元素它们的单质及其化合物的性质相似,如Li和Mg,试写出向BeCl2溶液中加入过量的NaOH溶液反应的化学方程式:BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O.
(7)图2是金属Ca和F所形成的某种合金的晶胞结构示意图,已知镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力.已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=5(填数值);氢在合金中的密度为0.083g•cm-3.
6.下列说法不正确的是( )
| A. | 已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 对于CaCO3(s)═CaO(s)+CO2(g) 任何温度下都不能自发进行 | |
| C. | 实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 | |
| D. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol. CO(g)+$\frac{1}{2}$O2(g)═CO2(g),△H=-283.0 kJ/mol. C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol. 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol |
3.下列热化学方程式书写正确的是( )
| A. | 2SO2+O2$\frac{\underline{\;500℃\;}}{V_{2}O_{5}}$2SO3△H=-196.6KJ•mol-1 | |
| B. | C(s)+O2(g)═CO2 (g)△H=+393.5KJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571kJ | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8KJ•mol-1 |
2.同温同压下,2H2(g)+O2(g)═2H2O(g)△H1;2H2(g)+O2(g)═2H2O(l)△H2,则△H1和△H2的关系是( )
| A. | △H1<△H2 | B. | △H1>△H2 | C. | △H1=△H2 | D. | 无法判断 |
1.与OH-有相同电子数和质子数的粒子是( )
0 156141 156149 156155 156159 156165 156167 156171 156177 156179 156185 156191 156195 156197 156201 156207 156209 156215 156219 156221 156225 156227 156231 156233 156235 156236 156237 156239 156240 156241 156243 156245 156249 156251 156255 156257 156261 156267 156269 156275 156279 156281 156285 156291 156297 156299 156305 156309 156311 156317 156321 156327 156335 203614
| A. | F- | B. | Cl- | C. | NH3 | D. | H2O |

 2011年9月29日我国成功发射的“天宫一号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分是氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:
2011年9月29日我国成功发射的“天宫一号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分是氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得: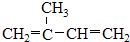 ⑤ClCH=CHCl ⑥
⑤ClCH=CHCl ⑥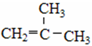 ⑦
⑦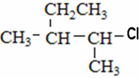 ⑧
⑧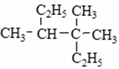 ⑨
⑨
 .
.