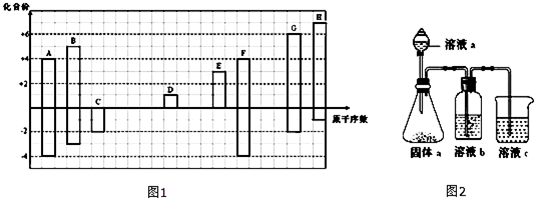
17.表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)⑧号元素的最高价氧化物对应的水化物的化学式为HClO4,③号元素氢化物的化学式为NH3,其电子式为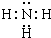
(2)写出⑤的最高价氧化物对应的水化物与⑥的最高价氧化物反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
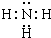
(2)写出⑤的最高价氧化物对应的水化物与⑥的最高价氧化物反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
16.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下发生反应:N2+3H2?2NH3.下列有关说法正确的是( )
| A. | 达到化学平衡时,有2molNH3生成 | |
| B. | 达到化学平衡时,正反应和逆反应的速率均为零 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量不再变化 | |
| D. | 达到化学平衡时,N2、H2和NH3的物质的量浓度之比为1:3:2 |
15.将6mol A 气体和3mol B气体置于3L的密闭容器中,混合后发生如下反应:2A(g)+B(g)═2C(g).若经2s后测得B的浓度为0.4mol/L,下列说法正确的是( )
| A. | 用物质A表示的反应速率为0.4mol/(L•s) | |
| B. | 用物质B表示的反应速率为0.4mol/(L•s) | |
| C. | 2 s时物质B的转化率为40% | |
| D. | 2 s时物质C的浓度为1.2 mol/L |
14.燃料电池是一种新型电池,它主要是利用燃料燃烧原理把化学能直接转化为电能,当以30%KOH溶液为电解质溶液,电极反应如下:2H2+4OH--4e-=4H2O,O2+2H2O+4e-=4OH-.据此作出判断,下列说法中不正确的是( )
| A. | 反应时负极附近pH增大 | B. | 电池总反应为2H2+O2=2H2O | ||
| C. | O2在正极发生还原反应 | D. | 工作时OH-向负极移动 |
13.下列实验中,不能观察到明显现象的是( )
| A. | 把绿豆大的钾投入水中 | |
| B. | 把除去氧化膜的镁带放入少量冷水中 | |
| C. | 把溴水滴加到KI溶液中,并加入少量四氯化碳溶液 | |
| D. | 把铜片和铁片紧靠在一起浸入稀硫酸中 |
12.下列关于反应速率的说法中,错误的是( )
| A. | 反应速率可衡量化学反应的快慢 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 增大反应物浓度、提高反应物温度都能增大反应速率 | |
| D. | 因是同一反应,所以用不同物质表示化学反应速率时,所得数值是相同的 |
11.已知反应X+Y=M+N为放热反应,对这个反应的下列说法中正确的是( )
| A. | X的能量一定高于M的能量 | |
| B. | 因为该反应为放热反应,故不需要加热就能进行 | |
| C. | X和Y的总能量一定低于M和N的总能量 | |
| D. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
10.下列化学反应属于吸热反应的是( )
0 156136 156144 156150 156154 156160 156162 156166 156172 156174 156180 156186 156190 156192 156196 156202 156204 156210 156214 156216 156220 156222 156226 156228 156230 156231 156232 156234 156235 156236 156238 156240 156244 156246 156250 156252 156256 156262 156264 156270 156274 156276 156280 156286 156292 156294 156300 156304 156306 156312 156316 156322 156330 203614
| A. | NH4Cl与Ba(OH)2•8H2O研磨 | B. | 生石灰溶于水 | ||
| C. | 镁与稀盐酸反应 | D. | 甲烷燃烧 |
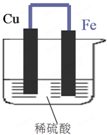 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.