9.下列实验操作中正确的是( )
| A. | 蒸馏实验中,温度计水银球应位于蒸馏烧瓶中液面以下 | |
| B. | 制备乙酸乙酯的实验中,导管末端要伸入饱和Na2CO3溶液液面下 | |
| C. | 分液操作中,待下层液体流出后,将上层液体从分液漏斗上口倒出 | |
| D. | 测定溶液pH时,可用pH试纸蘸取少量待测液并与标准比色卡比较 |
8.关于苯的叙述中错误的是( )
| A. | 苯在催化剂作用下能与液溴发生取代反应 | |
| B. | 苯不能使酸性高锰酸钾溶液褪色 | |
| C. | 苯在一定条件下能与氢气发生加成反应 | |
| D. | 苯分子是单双键交替的环状结构 |
6.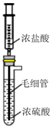 实验室用如图装置制备HCl气体.推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理分析不正确的是( )
实验室用如图装置制备HCl气体.推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理分析不正确的是( )
 实验室用如图装置制备HCl气体.推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理分析不正确的是( )
实验室用如图装置制备HCl气体.推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理分析不正确的是( )| A. | 混合时放热使HCl溶解度减小 | |
| B. | 浓硫酸具有吸水性,吸收了盐酸中水分 | |
| C. | 浓盐酸具有挥发性,利于HCl气体逸出 | |
| D. | 浓盐酸中HCl以分子形式存在,利于HCl气体逸出 |
1.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)实验结果表明,催化剂的催化效果与催化剂的表面积有关.
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(2)实验结果表明,催化剂的催化效果与催化剂的表面积有关.
20.实现下列变化时,需要克服相同类型作用力的是( )
0 156110 156118 156124 156128 156134 156136 156140 156146 156148 156154 156160 156164 156166 156170 156176 156178 156184 156188 156190 156194 156196 156200 156202 156204 156205 156206 156208 156209 156210 156212 156214 156218 156220 156224 156226 156230 156236 156238 156244 156248 156250 156254 156260 156266 156268 156274 156278 156280 156286 156290 156296 156304 203614
| A. | 水晶和干冰的熔化 | B. | 食盐和醋酸钠的熔化 | ||
| C. | 乙醇和HCl溶于水 | D. | HCl和NaCl溶于水 |
 A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
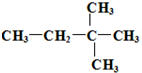
A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出). 用系统命名法命名该烃:2,3-二甲基戊烷.
用系统命名法命名该烃:2,3-二甲基戊烷.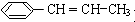 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式: .
. .
.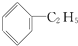 与
与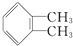
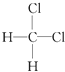 与
与
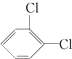 与
与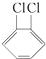
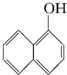 与
与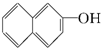
 由另一种烃D通过加成反应而制得,则烃D的可能的是
由另一种烃D通过加成反应而制得,则烃D的可能的是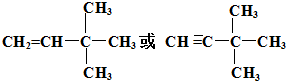 (任写一种可能的结构简式)
(任写一种可能的结构简式)