19.某元素构成的双原子单质分子有三种,其式量分别为158、160、162.在天然单质中,此三种单质的物质的量之比为1:1:1,由此推断以下结论中,正确的是( )
| A. | 此元素有三种同位素 | |
| B. | 其中一种同位素质量数为80 | |
| C. | 其中质量数为79的同位素原子占原子总数的$\frac{1}{3}$ | |
| D. | 此元素的单质的平均式量为160 |
17.2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g)是制备硫酸的重要反应.下列叙述中,正确的是( )
| A. | 催化剂V2O5不改变该反应的逆反应速率 | |
| B. | 增大反应体系的压强,反应速率不一定增大 | |
| C. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1mol/L、c2mol/L,则时间间隔t1min~t2min内,SO3(g)生成的平均速率为v=$\frac{{c}_{2}-{c}_{1}}{{t}_{2}-{t}_{1}}$mol/L•min |
16.反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g),在2L的密闭容器中进行,1min后,NH3减少了0.12mol,则该反应的化学反应速率表示正确的是( )
| A. | NH3:0.002 mol•L-1•s-1 | B. | H2O:0.0015 mol•L-1•s-1 | ||
| C. | NO:0.0015 mol•L-1•s-1 | D. | O2:0.00125 mol•L-1•s-1 |
15.已知反应A2+B2═2AB,破坏1mol A2中的化学键消耗的能量为Q1 kJ,破坏1mol B2中的化学键消耗的能量为Q2 kJ,形成1mol AB中的化学键释放的能量为Q3 kJ,则下列说法正确的是( )
| A. | 若A2和B2的总能量大于生成的AB的总能量,则反应放热 | |
| B. | 若A2和B2的总能量小于生成的AB的总能量,则反应放热 | |
| C. | 若该反应为放热反应,则Q1+Q2>Q3 | |
| D. | 若该反应为吸热反应,则Q1+Q2>Q3 |
14.对于可逆反应N2+3H2?2NH3下列各项所表示的反应速率最快的是( )
| A. | ν(N2)=0.02 mol•L-1•s-1 | B. | ν(H2)=0.2 mol•L-1•s-1 | ||
| C. | ν(H2)=0.6 mol•L-1•min-1 | D. | ν(NH3)=1.2 mol•L-1•min-1 |
12.1.01×105Pa,150℃时,将1L C2H4、2L C2H6与20L氧气混合并点燃,完全反应后氧气有剩余.当反应后的混合气体恢复到原条件时,气体体积为( )
| A. | 15L | B. | 20L | C. | 23L | D. | 24L |
11.下列反应中属于加成反应的是( )
| A. | 乙烯使溴水褪色 | |
| B. | 将苯滴入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使酸性KMnO4溶液褪色 | |
| D. | 甲烷与氯气混合,黄绿色消失 |
10.苯加溴水后,振荡,溴水层颜色变浅,这是由于( )
0 156097 156105 156111 156115 156121 156123 156127 156133 156135 156141 156147 156151 156153 156157 156163 156165 156171 156175 156177 156181 156183 156187 156189 156191 156192 156193 156195 156196 156197 156199 156201 156205 156207 156211 156213 156217 156223 156225 156231 156235 156237 156241 156247 156253 156255 156261 156265 156267 156273 156277 156283 156291 203614
| A. | 溴挥发了 | B. | 发生了取代反应 | ||
| C. | 苯萃取了溴水中的溴 | D. | 发生了加成反应 |
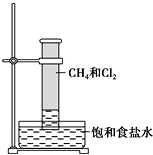 某课外活动小组利用如图所示装置探究甲烷与氯气的反应.根据题意,回答下列问题:
某课外活动小组利用如图所示装置探究甲烷与氯气的反应.根据题意,回答下列问题: