9.下列离子方程式正确的是( )
| A. | NaHS溶液水解的方程式为:HS-+H2O?S2-+H3O+ | |
| B. | 向H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH-+18O2↑ | |
| C. | 在100 mL 2 mol/L FeI2溶液中通入4.48 L氯气(标况下),充分反应:2I-+Cl2═I2+2Cl- | |
| D. | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ |
8.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

关于该固体混合物,下列说法正确的是( )

关于该固体混合物,下列说法正确的是( )
| A. | 一定含有Al,其质量为2.7g | |
| B. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 | |
| C. | 一定含有MgCl2和FeCl2 | |
| D. | 一定不含FeCl2,可能含有MgCl2和AlCl3 |
7.已知反应:A(g)+2B(g)?C(s)+D(?)△H<0,将A和B按下图比例充入一体积为10L的密闭容器中,经20s达到平衡,A、B物质浓度的变化曲线如下图所示.下列说法正确的是( )
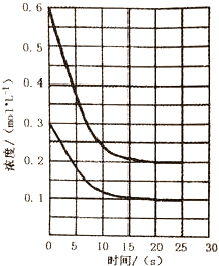

| A. | 从投料到20s时达到平衡,v(A)的反应速率为0.02mol•L-1•s-1 | |
| B. | 若该反应的化学平衡常数K=250,说明D的状态为气态 | |
| C. | 降低温度,有利于加快化学反应速率和提高反应的转化率 | |
| D. | 若D是固体且保持平衡的温度和压强不变,再向容器中充入3mol的B,则此时v正<v逆 |
6.二氧化硫的催化氧化是放热反应,下列关于接触法制硫酸的叙述中正确的是( )
| A. | 为防止催化剂中毒,炉气在进入接触室之前需要净化 | |
| B. | 为提高SO2的转化率,接触室内反应温度选定在400℃~500℃ | |
| C. | 为防止污染大气,从吸收塔出来的尾气常用稀氨水吸收 | |
| D. | 为提高SO3的吸收效率,用稀硫酸代替水吸收SO3. |
5.下列与化学有关的说法中错误的是( )
| A. | 侯氏制碱、肥皂的制取工艺过程中均应用了物质溶解度的差异 | |
| B. | 使用可再生资源、用超临界二氧化碳替代有机溶剂、注重原子的经济性、采用低能耗生产工艺等都是绿色化学的内容 | |
| C. | 石油分馏、煤的气化、海水晒盐、碱去油污、花生中提取花生油等过程都是物理变化 | |
| D. | 合金超导材料是指熔合两种或两种以上的金属元素并形成具有超导电性的超导材料,如铌一钛(Nb-Ti)合金,通常它的熔点一般比纯钛要高. |
3.下列说法正确的是( )
| A. | 同一主族相邻两个周期的元素的原子序数差为上一周期所含元素种类 | |
| B. | 短周期元素中同主族元素X的原子序数不可能是Y的2倍 | |
| C. | L层上的电子数为奇数的元素一定是主族元素 | |
| D. | 目前使用的元素周期表中,最长的周期含36种元素 |
2.表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:HClO4,碱性最强的化合物的电子式是: .
.
(2)最高价氧化物是两性氧化物的元素是Al;写出它的氧化物与氢氧化钠反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(3)用电子式表示元素④与⑥的化合物的形成过程: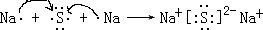
(4)表示①与⑦的化合物的电子式 ,该化合物是由极性(填“极性”“非极性”)键形成的.
,该化合物是由极性(填“极性”“非极性”)键形成的.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-(要求用离子符号表示).
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为:Cl2+H2O=HClO+H++Cl-.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)最高价氧化物是两性氧化物的元素是Al;写出它的氧化物与氢氧化钠反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(3)用电子式表示元素④与⑥的化合物的形成过程:
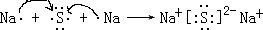
(4)表示①与⑦的化合物的电子式
 ,该化合物是由极性(填“极性”“非极性”)键形成的.
,该化合物是由极性(填“极性”“非极性”)键形成的.(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-(要求用离子符号表示).
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为:Cl2+H2O=HClO+H++Cl-.
1.向四个体积相同的密闭容器中分别充入一定量的SO2和O2,
甲:500℃,10mol SO2和5mol O2反应;
乙:500℃,V2O5作催化剂,10mol SO2和5mol O2反应;
丙:450℃,8mol SO2和5mol O2反应;
丁:500℃,8mol SO2和5mol O2反应,
开始反应时,按反应速率由大到小的排列顺序正确的是( )
甲:500℃,10mol SO2和5mol O2反应;
乙:500℃,V2O5作催化剂,10mol SO2和5mol O2反应;
丙:450℃,8mol SO2和5mol O2反应;
丁:500℃,8mol SO2和5mol O2反应,
开始反应时,按反应速率由大到小的排列顺序正确的是( )
| A. | 甲、乙、丙、丁 | B. | 乙、甲、丙、丁 | C. | 乙、甲、丁、丙 | D. | 丁、丙、乙、甲 |
20.已知2mol氢气完全燃烧生成水蒸气时放出能量484kJ,且氧气中1mol O═O键完全断裂时吸收能量496kJ,水蒸气中1mol H-O键形成时放出能量463kJ,则氢气中1mol H-H键断裂时吸收能量为( )
0 156092 156100 156106 156110 156116 156118 156122 156128 156130 156136 156142 156146 156148 156152 156158 156160 156166 156170 156172 156176 156178 156182 156184 156186 156187 156188 156190 156191 156192 156194 156196 156200 156202 156206 156208 156212 156218 156220 156226 156230 156232 156236 156242 156248 156250 156256 156260 156262 156268 156272 156278 156286 203614
| A. | 920 kJ | B. | 557 kJ | C. | 436 kJ | D. | 188 kJ |
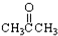 ③CH3CH2Br ④
③CH3CH2Br ④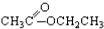 ⑤
⑤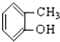 ⑥
⑥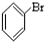 ⑦
⑦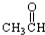 ⑧
⑧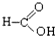 ⑨
⑨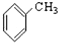 ⑩
⑩