6.试管内壁附着的以下物质用KOH溶液(必要时可加热)难以洗去的是( )
| A. | 硫 | B. | 油渍 | C. | 石炭酸 | D. | 酚醛树脂 |
5.25℃时,下列关于pH=2的醋酸溶液的叙述正确的是( )
| A. | 由水电离出的c(H+)=1.0×10-2mol•L-1 | |
| B. | 醋酸的电离平衡常数Ka=c(CH3COO-)•c(H+) | |
| C. | 若将溶液的温度升高到100℃,c(OH-)减小 | |
| D. | 加水稀释后H+的物质的量增加 |
4.我国汉书中记载:“高奴县有洧水,可燃”,沈括在《梦溪笔谈》对洧水的使用有如下描述:“予知其烟可用,试扫其烟为墨,黑光如漆,松墨不及也”,对上述史实记载分析正确的是( )
| A. | 该物质属于纯净物 | B. | 该物质可能属于无机化合物 | ||
| C. | 该物质是由同一类烃组成的混合物 | D. | 烟是该物质不完全燃烧的产物 |
3.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 80mL10mol/L的浓盐酸与足量的MnO2加热反应,产生Cl2分子数约为0.2NA | |
| B. | 一定条件下,将1molN2和3molH2混合,充分反应后转移电子数为6NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| D. | 常温常压下,等质量的CO和N2中含有原子数目均为2NA |
1.下列说法正确的是( )
| A. | 碘单质能升华是由于碘单质分子间的键能较小 | |
| B. | 键能越大,则含该键的分子受热越易分解为原子 | |
| C. | 燃料燃烧过程中,反应物的总能量总是高于生成物的总能量 | |
| D. | H-Cl键的键能为431kJ•mol-1,H-I键的键能为299kJ•mol-1,这说明HCl分子比HI分子稳定 |
20.pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值.如某溶液中某溶液的浓度为1×10-3mlo/L,则该溶液中该溶质的pC=-1g(1×10-3)=3.如图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5mlo/L,可认为该离子不存在).下列说法不正确的是( )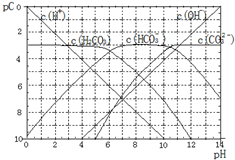

| A. | 某温度下,CO2饱和溶液的浓度是0.05mol•L-1,其中$\frac{1}{5}$的CO2转变为H2CO3,若此时溶液的pH约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度为0.1% | |
| B. | 25℃时,H2CO3一级电离平衡常数的数值Ka1=10-6 | |
| C. | 向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO${\;}_{3}^{2-}$)+c(OH-)+c(HCO${\;}_{3}^{-}$) | |
| D. | 25℃时,0.1mol/LNa2CO3中C(HCO${\;}_{3}^{-}$)比0.1mol/LH2CO3中C(HCO${\;}_{3}^{-}$)大 |
17.常温下,浓度均为0.1mlo•L-1的HX、HY溶液各20mL,分别用0.1mol•L-1的Na0H溶液滴定.溶液的pH与所用Na0H的体积V关系如图所示,下列推断不正确的是( )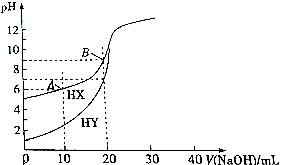
0 156086 156094 156100 156104 156110 156112 156116 156122 156124 156130 156136 156140 156142 156146 156152 156154 156160 156164 156166 156170 156172 156176 156178 156180 156181 156182 156184 156185 156186 156188 156190 156194 156196 156200 156202 156206 156212 156214 156220 156224 156226 156230 156236 156242 156244 156250 156254 156256 156262 156266 156272 156280 203614

| A. | 相同条件下,HX和HY中和碱的能力相同 | |
| B. | 常温下,HX的电离平衡常数K=1×10-9mol•L-1 | |
| C. | 点存在:c(X-)-c(HX)>c(H+)-c(0H-) | |
| D. | 向B点溶液通人HCl气体至中性:c(HX)+c(Cl-)+2c(X-)=0.2mol•L-1A |