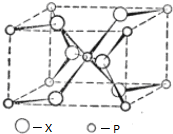
16.R、T、W、X、Y、Z都是短周期元素,且W、X、Y、Z的核电荷数依次增大.下表列出它们的性质和结构:
(1)Y原子的价电子排布式为3s1,T、X、Z的电负性由大到小的顺序为O>C>Si(用化学符号填空).
(2)WTR分子中的三个原子除W原子外均为8电子构型,根据电子云重叠方式的不同,分子里共价键的类型有σ键和π键.
(3)常温下,RW3是一种刺激性气味、易液化的气体.RW3极易溶于水的原因是NH3与H2O之间易形成氢键.
(4)将过量的RW3气体通入盛有硫酸铜溶液的试管里,现象为先产生蓝色沉淀,后沉淀消失,变成深蓝色的溶液.
| 元素编号 | 元素性质或原子结构 |
| R | 原子价电子排布式为nsnnpn+1 |
| T | 基态原子核外3个能级上有电子,且各能级上的电子数相等 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外p能级上的电子总数比s能级上的电子总数多2 |
(2)WTR分子中的三个原子除W原子外均为8电子构型,根据电子云重叠方式的不同,分子里共价键的类型有σ键和π键.
(3)常温下,RW3是一种刺激性气味、易液化的气体.RW3极易溶于水的原因是NH3与H2O之间易形成氢键.
(4)将过量的RW3气体通入盛有硫酸铜溶液的试管里,现象为先产生蓝色沉淀,后沉淀消失,变成深蓝色的溶液.
15.下列说法正确的是( )
| A. | 最外层电子排布为ns2的元素一定处于周期表IIA族 | |
| B. | 互为手性异构体的分子互为镜像 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 在晶体中有阳离子一定就有阴离子 |
14.下列有关说法不正确的是( )
| A. | 金属Po的晶体堆积模型是简单立方堆积,其配位数是8 | |
| B. | 原子晶体中原子以共价键结合,具有键能大,熔点高,硬度大的特点 | |
| C. | 氯化钠晶体中,每个晶胞中平均含有4个钠离子和4个氯离子 | |
| D. | 在冰晶体中,每一个水分子周围有4个水分子紧密相邻 |
13.下列不属于晶体的特点是( )
| A. | 无色透明的固体 | B. | 自范性 | C. | 固定的熔点 | D. | 各向异性 |
12.下列叙述正确的是( )
| A. | 2s轨道可以和3p轨道形成sp2杂化轨道 | |
| B. | 烯烃中的碳碳双键由l个σ键和l个π键组成 | |
| C. | 由极性键组成的分子,一定是极性分子 | |
| D. | 甲烷中sp3杂化轨道的构型是平面正方形 |
11.有关原子最外层电子排布为(n+1)sn(n+1)p n+1的元素及其化合物,下列叙述中不正确的是( )
| A. | 氢化物受热易分解 | |
| B. | 该元素是植物生长所需要的一种营养元素 | |
| C. | 其单质既有氧化性又有还原性 | |
| D. | 最高价氧化物对应的水化物是一种强酸 |
10.下列表达式错误的是( )
0 156073 156081 156087 156091 156097 156099 156103 156109 156111 156117 156123 156127 156129 156133 156139 156141 156147 156151 156153 156157 156159 156163 156165 156167 156168 156169 156171 156172 156173 156175 156177 156181 156183 156187 156189 156193 156199 156201 156207 156211 156213 156217 156223 156229 156231 156237 156241 156243 156249 156253 156259 156267 203614
| A. | 甲烷的电子式: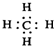 | |
| B. | 氮原子的L层电子的电子排布图: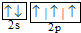 | |
| C. | 碳-12原子:${\;}_{6}^{12}$C | |
| D. | S2-的核外电子排布式:1s22s22p63s23p4 |
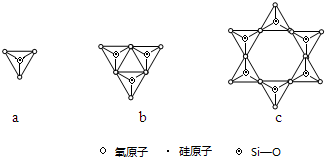
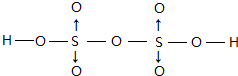 (配位键须注明).
(配位键须注明).