6.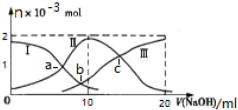 常温下,向10mL某浓度的H2SO3溶液中滴加0.2mol•L-1 NaOH溶液,含S微粒的物质的量变化曲线如图所示,下列有关说法正确的是( )
常温下,向10mL某浓度的H2SO3溶液中滴加0.2mol•L-1 NaOH溶液,含S微粒的物质的量变化曲线如图所示,下列有关说法正确的是( )
 常温下,向10mL某浓度的H2SO3溶液中滴加0.2mol•L-1 NaOH溶液,含S微粒的物质的量变化曲线如图所示,下列有关说法正确的是( )
常温下,向10mL某浓度的H2SO3溶液中滴加0.2mol•L-1 NaOH溶液,含S微粒的物质的量变化曲线如图所示,下列有关说法正确的是( )| A. | 曲线Ⅱ代表H2SO3的浓度 | |
| B. | V(NaOH)=10ml时,溶液温度最高,c(H2SO3)=0.1mol•L-1 | |
| C. | 水的电离程度大小:a点<b点<c点 | |
| D. | 若c点pH=6,则K2(H2SO3)=10-8 |
5.下列有关实验操作及原理正确的是( )
| A. | 用玻璃棒蘸取NaClO溶液,点在干燥的pH试纸上,证明HClO是弱酸 | |
| B. | 将一定量的FeCl3晶体、盐酸依次加入容量瓶中,配制一定物质的量浓度的FeCl3溶液 | |
| C. | 将Cu与浓硫酸反应剩余的液体加入到盛有蒸馏水的烧杯中,以证明反应生成了CuSO4 | |
| D. | 用乙醇、乙酸制取乙酸乙酯的过程中发现忘加碎瓷片,可立即补加 |
4.现有部分短周期元素的原子结构如表:
(1)写出X的元素符号:N,元素Y的最简单氢化物的化学式为CH4.
(2)Z元素原子的质量数为23.
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为H++OH-=H2O.
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式2CO2+2Na2O2=2Na2CO3+O2
(5)W、X、Y、Z为短周期内除稀有气体元素外的四种元素.它们的原子序数依次增大,其中只有Y是金属元素,Y的最外层电子数和W最外层电子数相等,Y、Z两元素的质子数之和为W、X两元素的质子数之和的3倍.由此可知元素W为H;X为O;Y 为Na;Z为S.上述元素中任意三种可组成盐,写出这些盐的化学式Na2SO4、Na2SO3、Na2S2O3、NaHS.
| 元素符 号 | 元素原子结构 |
X | 原子结构示意图为 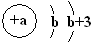 |
| Y | 最外层电子数是次外层电子数的2倍 |
Z | 原子核内含有12个中子,且其离子的结构示意图为  |
(2)Z元素原子的质量数为23.
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为H++OH-=H2O.
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式2CO2+2Na2O2=2Na2CO3+O2
(5)W、X、Y、Z为短周期内除稀有气体元素外的四种元素.它们的原子序数依次增大,其中只有Y是金属元素,Y的最外层电子数和W最外层电子数相等,Y、Z两元素的质子数之和为W、X两元素的质子数之和的3倍.由此可知元素W为H;X为O;Y 为Na;Z为S.上述元素中任意三种可组成盐,写出这些盐的化学式Na2SO4、Na2SO3、Na2S2O3、NaHS.
3.1999年是人造元素丰收年,一年间得到了核电荷数分别为114、116和118三种新元素,已知核电荷数为118的新元素的一种原子的质量数为293,则该原子中子与电子数之差为( )
| A. | 0 | B. | 57 | C. | 118 | D. | 175 |
1.如表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号,下同).
(2)NH3电子式是: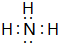 ;
;
(3)④、⑤、⑥的原子半径由大到小的顺序为Na>Al>S.(用元素符号表示)
(4)①、⑥、⑦的最高价氧化物对应水化物的酸性最强的是HClO4>H2SO4>H2CO3.(用化学式表示)
(5)写出 ⑥的原子结构示意图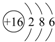 ;
;
(6)③氢化物的沸点大于(填“大于”、“小于”)⑥的氢化物的沸点.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)NH3电子式是:
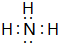 ;
;(3)④、⑤、⑥的原子半径由大到小的顺序为Na>Al>S.(用元素符号表示)
(4)①、⑥、⑦的最高价氧化物对应水化物的酸性最强的是HClO4>H2SO4>H2CO3.(用化学式表示)
(5)写出 ⑥的原子结构示意图
 ;
;(6)③氢化物的沸点大于(填“大于”、“小于”)⑥的氢化物的沸点.
19.下列化学反应△H最小的是( )
| A. | NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l);△H1 | |
| B. | NaOH(aq)+$\frac{1}{2}$H2SO4(浓)═$\frac{1}{2}$Na2SO4(aq)+H2O(l);△H4 | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq )+H2O(l);△H2 | |
| D. | CH3COOH(aq)+NaOH(aq)═CH3COONa (aq )+H2O(l);△H3 |
18.下列反应中,属于吸热反应的是( )
| A. | 锌与硫酸反应制取氢气 | B. | NaOH与HCl的反应 | ||
| C. | 高温煅烧石灰石 | D. | 铝与稀盐酸 |
17.PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍.Z是常见的金属,其原子的电子层数等于主族序数.W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
0 156072 156080 156086 156090 156096 156098 156102 156108 156110 156116 156122 156126 156128 156132 156138 156140 156146 156150 156152 156156 156158 156162 156164 156166 156167 156168 156170 156171 156172 156174 156176 156180 156182 156186 156188 156192 156198 156200 156206 156210 156212 156216 156222 156228 156230 156236 156240 156242 156248 156252 156258 156266 203614
| A. | 熔沸点:X2Y>X2R | |
| B. | WY2能与碱反应,但不能与任何酸反应 | |
| C. | Z与Y形成的化合物不能作为耐高温材料 | |
| D. | 原子半径按X、Y、Z、R、W的顺序依次减小 |