16.下列反应的离子方程式书写正确的是( )
| A. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 用FeCl3溶液腐蚀印刷电路板:2Fe3++Cu═2Fe2++Cu2+ | |
| C. | 钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气跟水反应:Cl2+H2O═2H++Cl-+ClO- |
15.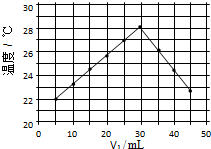 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )| A. | 做该实验时环境温度为22℃ | |
| B. | 该实验表明化学能可能转化为热能 | |
| C. | NaOH溶液的浓度约为1.5mol/L | |
| D. | 该实验表明有水生成的反应都是放热反应 |
14.某元素的一种核素${\;}_{N}^{A}$X,它与2H原子组成HmX分子,在a g HmX中所含电子的物质的量是( )
| A. | $\frac{a}{A}$(m+N)mol | B. | $\frac{a}{A+2m}$ (A-N+m)mol | C. | $\frac{a}{A+m}$(A-N+m)mol | D. | $\frac{a}{A+2m}$(m+N)mol |
13.下列各组粒子中粒子半径由小到大的是( )
| A. | O2- Na+Mg2+Al3+ | B. | O P S Cl | ||
| C. | A l3+Mg2+ Na+ F- | D. | K+ Mg2+ Al3+ H+ |
12.下列说法正确的是( )
| A. | 任何化学反应都伴随能量变化 | |
| B. | 化学反应中的能量变化都表现为热量的变化 | |
| C. | CH4的完全燃烧过程中放出热量,属于放热反应,即反应物的总能量低于生成物的总能量 | |
| D. | Ba(OH)2•8H2O与NH4Cl反应过程中吸收热量,属于吸热反应,即反应物的总能量高于生成物的总能量 |
11.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 7.8 g Na2O2与足量水反应转移的电子数为0.1NA | |
| B. | 常温常压下,22.4LCH4中含有的氢原子数为4NA | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.2NA | |
| D. | 12.0 g熔融的NaHSO4中含有0.1NA个Na+、0.1NA个H+和0.1NA个SO42- |
10.随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现.下列有关说法中,正确的是( )
| A. | N5+中含有36个电子 | B. | C60的摩尔质量为720 | ||
| C. | H2与H3互为同位素 | D. | O2与O4属于同素异形体 |
9.下列两种物质,只有在加热的条件下才能反应并产生气体的是( )
| A. | Cu+H2SO4(稀) | B. | Cu+HNO3(浓) | C. | Fe+HNO3(稀) | D. | C+H2SO4(浓) |
8.将下列溶液置于敞口容器中,溶液质量会出现增重的是( )
| A. | 浓氨水 | B. | 浓盐酸 | C. | 浓H2SO4 | D. | 浓硝酸 |
7.下列关于硅和硅的化合物性质的叙述,正确的是( )
0 156071 156079 156085 156089 156095 156097 156101 156107 156109 156115 156121 156125 156127 156131 156137 156139 156145 156149 156151 156155 156157 156161 156163 156165 156166 156167 156169 156170 156171 156173 156175 156179 156181 156185 156187 156191 156197 156199 156205 156209 156211 156215 156221 156227 156229 156235 156239 156241 156247 156251 156257 156265 203614
| A. | 二氧化硅是酸性氧化物,不跟任何酸起反应 | |
| B. | 二氧化硅的化学键是共价键,可溶于水制得硅酸 | |
| C. | 根据CO2通入水玻璃中可制得硅酸,可知碳酸的酸性比硅酸强 | |
| D. | 硅在常温下能跟氢气起反应生成SiH4 |