6.下列有机物的命名正确的是( )
| A. | 二溴乙烷: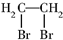 | B. | 3-乙基-1-丁烷: | ||
| C. | 2,2,3-三甲基戊烷: | D. | 2-甲基-2,4-己二烯: |
5.${\;}_{6}^{13}$C-NMR(核磁共振)可用于含碳化合物的结构分析.下列有关${\;}_{6}^{13}$C的说法正确的是( )
| A. | ${\;}_{6}^{13}$C的质量数是13,原子序数是6,核内有6个中子 | |
| B. | ${\;}_{6}^{13}$C的是碳的一种核素,与${\;}_{6}^{12}$C互为同位素 | |
| C. | 碳元素的相对原子质量为13 | |
| D. | ${\;}_{6}^{13}$C的与金刚石、石墨、C60等互为同素异形体 |
4.下列化学用语正确的是( )
| A. | 二氧化碳分子的比例模型 | B. | NH3的电子式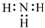 | ||
| C. | 乙烷的分子式 CH3CH3 | D. | 丙烯的结构简式 CH3CH=CH2 |
2.某学生在做元素性质与原子结构关系的实验时,设计了一套实验方案,并记录了有关的实验现象.请帮助该学生整理并完成实验报告.
(1)实验目的:探究同一主族元素性质的递变规律.
(2)实验用品:仪器:试管、胶头滴管.
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳.
(3)实验内容(在下表横线中填写相关内容).
(4)实验结论:同主族元素从上到下元素原子的得电子能力逐渐减弱.
(5)问题和讨论.
①上述两个实验中发生反应的离子方程式分别为Cl2+2Br-=Br2+2Cl-、2I-+Br2=2Br-+I2.
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱.试列举两项事实说明氟的非金属性比氯的强:HF的稳定性比HCl强、F2能置换出水中的氧,而Cl2不能置换出水中的氧.
(1)实验目的:探究同一主族元素性质的递变规律.
(2)实验用品:仪器:试管、胶头滴管.
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳.
(3)实验内容(在下表横线中填写相关内容).
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层 呈橙红色 |
| ② | 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层 呈紫红色 |
(5)问题和讨论.
①上述两个实验中发生反应的离子方程式分别为Cl2+2Br-=Br2+2Cl-、2I-+Br2=2Br-+I2.
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱.试列举两项事实说明氟的非金属性比氯的强:HF的稳定性比HCl强、F2能置换出水中的氧,而Cl2不能置换出水中的氧.
20.下列关于浓硫酸的叙述中,正确的是( )
| A. | 浓硫酸在常温下能够使铁、铝等金属表面形成氧化膜而钝化 | |
| B. | 浓硫酸在常温下可迅速与碳反应放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气、硫化氢等气体 | |
| D. | 浓硫酸具有吸水性,因而能使蔗糖炭化 |
19.下列物质见光不会分解的是( )
| A. | HClO | B. | AgNO3 | C. | HNO3 | D. | NH4Cl |
18.下列说法正确的是( )
| A. | 铵盐化学性质都很稳定 | |
| B. | 锌片与稀硝酸反应可制得氢气 | |
| C. | 雷雨天气时空气中能生成少量的氮氧化物 | |
| D. | O2、NO、NO2都能用浓硫酸干燥,且通常情况下能共存 |
17.高温下硫酸亚铁发生如下反应:2FeSO4=Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钙溶液中,得到的沉淀是( )
0 156066 156074 156080 156084 156090 156092 156096 156102 156104 156110 156116 156120 156122 156126 156132 156134 156140 156144 156146 156150 156152 156156 156158 156160 156161 156162 156164 156165 156166 156168 156170 156174 156176 156180 156182 156186 156192 156194 156200 156204 156206 156210 156216 156222 156224 156230 156234 156236 156242 156246 156252 156260 203614
| A. | CaSO4和CaSO3 | B. | CaSO4 | C. | CaS | D. | CaSO3 |
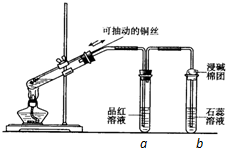 某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:
某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题: