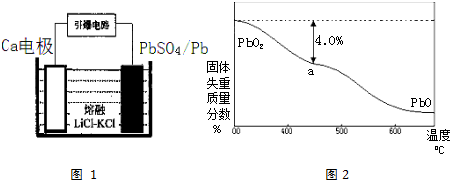
6.下列陈述 I、陈述 II均正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2能使溴水褪色 | SO2具有还原性 |
| B | NH3能使酚酞溶液变红 | NH3可用于设计喷泉 |
| C | SiO2能与氢氟酸、碱反应 | SiO2是两性氧化物 |
| D | 晶体Si熔点高硬度大 | 晶体Si可用作半导体材料 |
| A. | A | B. | B | C. | C | D. | D |
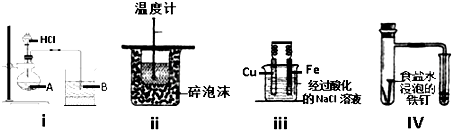
5.下列实验不能达到预期目的是( )
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、Al Cl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | NaCO3溶液中加入稀H2SO4 | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与盐酸反应 | 比较铁、铜的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
4.几种短周期元素的原子半径及主要化合物如表所示:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +3、+5、-3 | -2 |
| A. | Z的最高价氧化物对应水化物与其氢化物能发生化合反应生成离子化合物 | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 相同条件下,X、Y的单质分别与盐酸反应时,后者反应剧烈些 |
3.氯气是一种重要的工业原料.工业上利用反应3Cl2+8NH3=N2+6NH4Cl检查氯气管道是否漏气.下列说法错误的是( )
| A. | 若管道漏气则遇氨就会产生白烟 | |
| B. | 该反应利用了Cl2的强氧化性 | |
| C. | 实验室可用 NH4Cl受热分解制取NH3 | |
| D. | 生成1 molN2有6 mol电子转移 |
2.原子结构决定元素的性质,下列说法中正确的是( )
| A. | Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小 | |
| B. | 在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的是H2O | |
| C. | 第二周期元素的最高正化合价都等于其原子的最外层电子数 | |
| D. | 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 |
20. 据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).
据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).
(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是CH4•nH2O=CH4↑+nH2O.
(2)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油.
①在101KPa时,1.6g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64kJ.则甲烷与H2O(g)反应的热化学方程式:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1.
②CH4不完全燃烧也可制得合成气:CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g);
△H=-35.4kJ•mol-1.则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为②(填序号);原因是选择CH4不完全燃烧,制合成气体时,放出热量,同时得到CO:H2为1:2,能恰好完全反应合成甲醇.
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)=CH3OH(g)△H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)=CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算△H1=-99kJ•mol-1,已知△H2=-58kJ•mol-1,则△H3=+41kJ•mol-1.
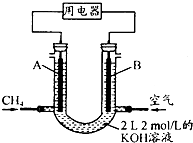
(4)可燃冰中CH4的其它用途是,将CH4设计成燃料电池,其利用率更高,装置示意图(A、B为多孔性碳棒).持续通人甲烷,在标准状况下,消耗甲烷体积VL.
①O<V≤44.8L时,电池总反应方程式为CH4+2O2+2KOH=K2CO3+3H2O,
②44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-.
 据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).
据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是CH4•nH2O=CH4↑+nH2O.
(2)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油.
①在101KPa时,1.6g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64kJ.则甲烷与H2O(g)反应的热化学方程式:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1.
②CH4不完全燃烧也可制得合成气:CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g);
△H=-35.4kJ•mol-1.则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为②(填序号);原因是选择CH4不完全燃烧,制合成气体时,放出热量,同时得到CO:H2为1:2,能恰好完全反应合成甲醇.
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)=CH3OH(g)△H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)=CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1 076 | 465 | 413 |
(4)可燃冰中CH4的其它用途是,将CH4设计成燃料电池,其利用率更高,装置示意图(A、B为多孔性碳棒).持续通人甲烷,在标准状况下,消耗甲烷体积VL.
①O<V≤44.8L时,电池总反应方程式为CH4+2O2+2KOH=K2CO3+3H2O,
②44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-.
19.某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸进行中和热的测定.
Ⅰ.配制0.50mol•L-1NaOH溶液
(1)配制0.50mol•L-1NaOH溶液时,需要使用的玻璃仪器除量筒、烧杯、玻璃棒外,还有250ml容量瓶、胶头滴管.
(2)若实验中约需要240ml0.50mol•L-1NaOH溶液,则应用量筒量取2.5mol•L-1NaOH溶液的体积为50.0ml.
Ⅱ.测定中和热
取60mL NaOH溶液和40mL硫酸溶液进行实验,实验数据如表.
(3)近似认为0.50mol•L-1NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,反应后溶液的比热容为4.18J/(g•℃),则中和热△H=-55.7kJ/mol.(结果保留一位小数)
(4)上述实验数值结果与57.3kJ•mol-1有偏差,产生此偏差的原因可能ad(填字母).
a.实验装置保温、隔热效果差
b.量取40mL0.50mol•L-1硫酸时俯视读数
c.硫酸倒入小烧杯时,有少量硫酸溅出
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钡溶液、稀氨水分别和1L 0.50mol/L的稀硫酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3由大到小的关系为△H3>△H1>△H2.
Ⅰ.配制0.50mol•L-1NaOH溶液
(1)配制0.50mol•L-1NaOH溶液时,需要使用的玻璃仪器除量筒、烧杯、玻璃棒外,还有250ml容量瓶、胶头滴管.
(2)若实验中约需要240ml0.50mol•L-1NaOH溶液,则应用量筒量取2.5mol•L-1NaOH溶液的体积为50.0ml.
Ⅱ.测定中和热
取60mL NaOH溶液和40mL硫酸溶液进行实验,实验数据如表.
| 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | ||
| H2SO4 | NaOH | 平均值 (保留小数点后一位) | ||
| 1 | 26.3 | 26.0 | 26.1 | 30.1 |
| 2 | 27.0 | 27.3 | 27.2 | 33.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.5 | 26.2 | 26.3 | 30.4 |
(4)上述实验数值结果与57.3kJ•mol-1有偏差,产生此偏差的原因可能ad(填字母).
a.实验装置保温、隔热效果差
b.量取40mL0.50mol•L-1硫酸时俯视读数
c.硫酸倒入小烧杯时,有少量硫酸溅出
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钡溶液、稀氨水分别和1L 0.50mol/L的稀硫酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3由大到小的关系为△H3>△H1>△H2.
17.根据下列事实:
(1)X+Y2+═X2++Y;
(2)Z+2H2O(冷)═Z(OH)2+H2↑;
(3)由Y、W电极组成的原电池,电极反应为:W2++2e-═W,Y-2e2-═Y2+.
可知X、Y、Z、W的还原性由强到弱的顺序是( )
0 156062 156070 156076 156080 156086 156088 156092 156098 156100 156106 156112 156116 156118 156122 156128 156130 156136 156140 156142 156146 156148 156152 156154 156156 156157 156158 156160 156161 156162 156164 156166 156170 156172 156176 156178 156182 156188 156190 156196 156200 156202 156206 156212 156218 156220 156226 156230 156232 156238 156242 156248 156256 203614
(1)X+Y2+═X2++Y;
(2)Z+2H2O(冷)═Z(OH)2+H2↑;
(3)由Y、W电极组成的原电池,电极反应为:W2++2e-═W,Y-2e2-═Y2+.
可知X、Y、Z、W的还原性由强到弱的顺序是( )
| A. | X>Z>Y>W | B. | Z>W>X>Y | C. | Z>X>Y>W | D. | Z>Y>X>W |