5.NA为阿伏加德罗常数的值,下列叙述一定正确的是( )
| A. | 0.1mol铜粉在0.05mol氯气中充分燃烧,转移电子数为0.2NA | |
| B. | 常温常压下,22.4L氙气中含有NA个氙分子 | |
| C. | 一定量的浓H2SO4与0.1molMg恰好完全反应,生成SO2为0.1NA | |
| D. | 标准状况下,22.4L由SO2和O3组成的混合气体中含有3NA个原子 |
4.下列实验操作、实验现象和解释或结论错误的是( )
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将铁片放入浓硫酸中 | 无明显现象 | 铁片发生了钝化 |
| B | 将SO2通入Na2CO3溶液中,将产生的气体再通入Na2SiO3溶液中 | 有白色沉淀生成 | 证明酸性: H2SO3>H2CO3>H2SiO3 |
| C | 向含有Fe3+的溶液中滴加KSCN溶液 | 溶液变红色 | 有Fe(SCN)3生成 |
| D | 向KOH溶液中滴加FeCl3溶液 | 有红褐色沉淀生成 | OH-+Fe3+=Fe(OH)3↓ |
| A. | A | B. | B | C. | C | D. | D |
19.短周期元素A、B、C、D、E的原子序数依次增大,其中A元素的原子核外电子数、核外电子层数和最外层电子数均相等.B、C、D、E在元素周期表中的相对位置如图1所示,其中E的单质的水溶液具有漂白性.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的若干种元素组成(只有M分子同时含有三种元素),甲、乙为非金属单质,M、W、X、Y、Z均为化合物,W是C2A4型共价化合物,X分子中含有10个电子,它们之间的相互转化关系如表所示.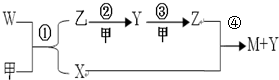
(1)写出元素名称B碳 E氯
(2)A、C、D三种元素组成的盐中,化学键类型为离子键、共价键
(3)乙的电子式为
(4)反应④的化学方程式为3NO2+H2O=2HNO3+NO,还原产物为NO
(5)W作火箭燃料时,氧化剂可以是Z,0.25mol的W气体完全和足量的Z气体反应生成乙和X,转移的电子为1mol.
0 156056 156064 156070 156074 156080 156082 156086 156092 156094 156100 156106 156110 156112 156116 156122 156124 156130 156134 156136 156140 156142 156146 156148 156150 156151 156152 156154 156155 156156 156158 156160 156164 156166 156170 156172 156176 156182 156184 156190 156194 156196 156200 156206 156212 156214 156220 156224 156226 156232 156236 156242 156250 203614

| B | C | D | |
| E |
(2)A、C、D三种元素组成的盐中,化学键类型为离子键、共价键
(3)乙的电子式为

(4)反应④的化学方程式为3NO2+H2O=2HNO3+NO,还原产物为NO
(5)W作火箭燃料时,氧化剂可以是Z,0.25mol的W气体完全和足量的Z气体反应生成乙和X,转移的电子为1mol.

 ,
, .
.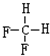 和
和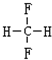
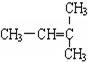 和CH2=CH-CH3
和CH2=CH-CH3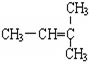 和
和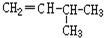
 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/L的硫酸溶液中,乙同学将电极放入6mol/L的NaOH溶液中,实验装置如图所示:
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/L的硫酸溶液中,乙同学将电极放入6mol/L的NaOH溶液中,实验装置如图所示: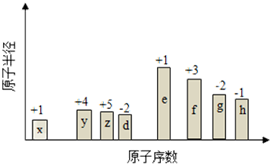 随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或 最低负价的变化如图所示. 根据判断出的元素回答问题:
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或 最低负价的变化如图所示. 根据判断出的元素回答问题: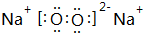 ,0.10mol该化合物与足量水反应时转移的电子数为6.02×1022.
,0.10mol该化合物与足量水反应时转移的电子数为6.02×1022.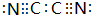 ,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是(CN)2+2NaOH=NaCN+NaCNO+H2O.
,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是(CN)2+2NaOH=NaCN+NaCNO+H2O.