13.目前人工合成高效青蒿素主要采用青蒿酸为原料半合成法.青蒿酸的结构简式如图A所示.下列有关说法正确的是( )
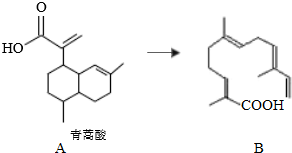

| A. | 青蒿酸的分子式为C15H20O2 | |
| B. | 1mol青蒿酸最多可与3molH2加成 | |
| C. | 青蒿酸与B互为同分异构体 | |
| D. | 苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体只有2种 |
12.下列选用的相关仪器,用品不符合实验要求的是( )
| 选项 | 实验 | 仪器用品 |
| A | 准确量取19.01mL水 | 25mL酸式滴定管 |
| B | 新制氯水的保存 | 带玻璃塞的棕色细口瓶 |
| C | 测定0.1mol•L-1的Na2CO3溶液的pH | 镊子、pH试纸、表面皿 |
| D | 分离水和乙酸乙酯 | 分液漏斗、烧杯 |
| A. | A | B. | B | C. | C | D. | D |
11.有机物X的分子式为C3H6O2,发生酸性水解后得到一元羧酸Y和一元醇Z,已知Y和Z的相对分子质量相等,则下列叙述错误的是( )
| A. | X的结构简式为HCOOCH2CH3 | B. | Y的分子中不含-CH3(甲基) | ||
| C. | Z不具有氧化性 | D. | Z分子中含有甲基且具有还原性 |
9.“凯氏定氮法”是测定化合物或混合物中总氮量的一种方法.近来,尿素化肥“金坷垃”在互联网上爆红.红星中学的化学实验小组成员想通过“凯氏定氮法”实验测定化肥“金坷垃”中的实际尿素含量,已检验它是否确实有网上所说的神奇功效.
实验流程如下:
金坷垃$→_{加热}^{辅助试剂}$(NH4)2SO4溶液$→_{吹出}^{NaOH}$NH3$→_{吸收}^{H_{3}BO_{3}}$(NH4)2B4O7溶液→用标准盐酸滴定
步骤:①取10.00g“金坷垃”尿素[CO(NH2)2]化肥溶于水,定容至100mL;
②在烧杯中加入10.00mL步骤①中得到的金坷垃水溶液和辅助试剂,加热充分反应;
③将反应液转移到大试管中;
④按如图2装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
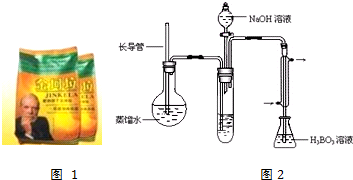
⑤取下锥形瓶,滴加指示剂,用0.2500mol•L-1盐酸标准液滴定;
⑥重复实验操作.
数据记录如表1:
表1
回答下列问题:
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl.
(2)步骤③的实验装置中需要加热的仪器是圆底烧瓶(填仪器名称),长导管的作用是作为安全管,防止装置中压力过大而发生危险;防止冷却时发生倒吸.
(3)编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸,理由是空白、等量对照以消除其他试剂、实验操作等因素引起的误差.
(4)通过计算可得“金坷垃”化肥中的氮含量为117.67-3.5x克/每千克化肥(用含x的代数式表示,要求化简).我国农业用尿素的标准为:
表2
总尿素含量低于46.0%的为不合格品.若x=2.77,则根据上述测定,可以确定“金坷垃”尿素化肥属于不合格品级别.
实验流程如下:
金坷垃$→_{加热}^{辅助试剂}$(NH4)2SO4溶液$→_{吹出}^{NaOH}$NH3$→_{吸收}^{H_{3}BO_{3}}$(NH4)2B4O7溶液→用标准盐酸滴定
步骤:①取10.00g“金坷垃”尿素[CO(NH2)2]化肥溶于水,定容至100mL;
②在烧杯中加入10.00mL步骤①中得到的金坷垃水溶液和辅助试剂,加热充分反应;
③将反应液转移到大试管中;
④按如图2装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);

⑤取下锥形瓶,滴加指示剂,用0.2500mol•L-1盐酸标准液滴定;
⑥重复实验操作.
数据记录如表1:
表1
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.90 |
| 3 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | x |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl.
(2)步骤③的实验装置中需要加热的仪器是圆底烧瓶(填仪器名称),长导管的作用是作为安全管,防止装置中压力过大而发生危险;防止冷却时发生倒吸.
(3)编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸,理由是空白、等量对照以消除其他试剂、实验操作等因素引起的误差.
(4)通过计算可得“金坷垃”化肥中的氮含量为117.67-3.5x克/每千克化肥(用含x的代数式表示,要求化简).我国农业用尿素的标准为:
表2
| 级别 | 优等品 | 一等品 | 合格品 |
| 总尿素含量%≥ | 46.4 | 46.2 | 46.0 |
8.纳米CdSe(硒化镉)可用作光学材料.在一定条件下,由Na2SO3和Se反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒.流程图如下:
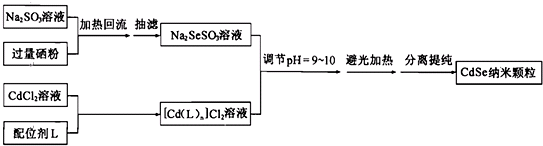
已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )

已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )
| A. | 在分离提纯CdSe时一般向溶液中加入丙酮,以增强溶剂极性,有利于CeSe的沉淀,提高收率 | |
| B. | 一般可用NaOH调节Na2SeSO3溶液的pH值,在此过程中会有HSe-和HSO3-生成 | |
| C. | 该纳米颗粒不能使用常压过滤或者减压过滤分离,因为其易在滤纸表面形成一层致密而厚实的膜,阻碍溶剂的通过 | |
| D. | 改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒;且若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法 |
7.下列关于化学实验的说法正确的是( )
| A. | 分离物质的量之比为1:6的氯化钠和硝酸钾混合物时,可先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得到硝酸钾晶体;将母液加热至有大量晶体析出后,用余热蒸干,得氯化钠晶体 | |
| B. | 在“反应热的测量和计算”实验时须先将用于实验的等体积等物质的量的稀NaOH和稀HCl溶液置于相同温度(一般为25℃)下保温一段时间后再混合 | |
| C. | 在电化学实验中常使用碳电极,实验室一般采用多孔碳棒作为碳电极.有些电化学反应中的气体产物可以自由填充在多孔碳棒的疏松空隙中,从而降低反应池的极性,提高电流效率 | |
| D. | 在实验中观察到的物质的颜色可能会与其理论颜色有一定的偏差,如通过Cu和浓HNO3反应制得的Cu(NO3)2溶液中因溶有少量NO2而显黄色,苯酚因被空气中的O2氧化而显粉红色. |
6.已知:①CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=-a kJ/mol
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-b kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-c kJ/mol
④H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-d kJ/mol
下列叙述不正确的是( )
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-b kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-c kJ/mol
④H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-d kJ/mol
下列叙述不正确的是( )
| A. | 由上述热化学方程式可知d>c | |
| B. | H2的燃烧热为d kJ/mol | |
| C. | CH3OH(g)═CO(g)+2H2(g)△H=(b+2c-a)kJ/mol | |
| D. | 当CO和H2的物质的量之比为1:2时,其完全燃烧生成CO2和H2O(l)时,放出Q kJ热量,则混合气中CO的物质的量为$\frac{Q}{b+2c}$mol |
5.下列有关实验设计、观察或记录、结论或解释都正确的是( )
0 156042 156050 156056 156060 156066 156068 156072 156078 156080 156086 156092 156096 156098 156102 156108 156110 156116 156120 156122 156126 156128 156132 156134 156136 156137 156138 156140 156141 156142 156144 156146 156150 156152 156156 156158 156162 156168 156170 156176 156180 156182 156186 156192 156198 156200 156206 156210 156212 156218 156222 156228 156236 203614
| 选项 | 实验设计 | 观察或记录 | 结论或解释 |
| A | 将浓硝酸分多次加入Cu和稀硫酸的混合液中 | 产生红棕色气体 | 浓硝酸的还原产物是NO2 |
| B | 测某铵盐溶液的pH | pH>7 | NH4+水解生成NH3•H2O,使溶液显碱性 |
| C | 用湿润的淀粉碘化钾试纸检验某气体 | 试纸变蓝 | 该气体一定是Cl2 |
| D | 将20mL pH均为1的盐酸和醋酸分别加水稀释至pH为3 | 醋酸的体积变化大 | 醋酸是弱酸 |
| A. | A | B. | B | C. | C | D. | D |
 .
. .
.