13.化学与社会、科学、技术、环境等有密切关系.下列说法正确的是( )
| A. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 | |
| B. | 含乙醇、NaClO、H2O2等消毒液均可以将病毒氧化而达到消毒目的 | |
| C. | 有机玻璃受热软化,易于加工成型,是一种硅酸盐材料 | |
| D. | 处理废水时,加入明矾作为消毒剂除去水中的细菌 |
10. 有A、B、C、D四种含14个电子的粒子,其结构特点如下:
有A、B、C、D四种含14个电子的粒子,其结构特点如下:
(1)某元素的原子核外电子数比A元素原子核外电子数多2,则该元素在周期表中的位置为第三周期第VIA族.工业上常以焦炭、A元素的氧化物为原料制取单质A,用化学方程式表示其原理SiO2+2C $\frac{\underline{\;高温\;}}{\;}$ Si+2CO↑.
(2)在101kPa,25℃时,42g B完全燃烧放出424.5kJ的热量,写出表示B的燃烧热的热化学方程式:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0 kJ/mol.
(3)32g 由D与钙离子组成的化合物中,含有的共用电子对数为9.03×1023.
(4)组成C的元素与另一短周期元素组成的分子的球棍模型如图所示.已知分子中所有原子的最外层均达到8电子稳定结构,原子间均以单键相连接.下列有关说法中错误的是C.
A.X原子为组成C的元素原子
B.该分子中,既含极性键,又含非极性键
C.Y原子可能为氢原子
D.从圆球的相对大小来分析,该分子可能为N2F4
(5)甲是组成C的元素最简单的气态氢化物.
①一定条件下,甲在恒容密闭容器中发生分解反应(正反应方向为吸热反应)并达平衡后,仅改变表中反应条件x,下列各项中y随x的增大而增大的是bc(填序号).
②甲与空气可以构成一种环保型燃料电池,电解质溶液是KOH,其负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
 有A、B、C、D四种含14个电子的粒子,其结构特点如下:
有A、B、C、D四种含14个电子的粒子,其结构特点如下:| 粒子代码 | A | B | C | D |
| 原子核数目 | 单核 | 不同元素构成的两核 | 同种元素构成的两核 | 同种元素构成的两核 |
| 粒子所带电荷数 | 0 | 0 | 0 | 两个负电荷 |
(2)在101kPa,25℃时,42g B完全燃烧放出424.5kJ的热量,写出表示B的燃烧热的热化学方程式:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0 kJ/mol.
(3)32g 由D与钙离子组成的化合物中,含有的共用电子对数为9.03×1023.
(4)组成C的元素与另一短周期元素组成的分子的球棍模型如图所示.已知分子中所有原子的最外层均达到8电子稳定结构,原子间均以单键相连接.下列有关说法中错误的是C.
A.X原子为组成C的元素原子
B.该分子中,既含极性键,又含非极性键
C.Y原子可能为氢原子
D.从圆球的相对大小来分析,该分子可能为N2F4
(5)甲是组成C的元素最简单的气态氢化物.
①一定条件下,甲在恒容密闭容器中发生分解反应(正反应方向为吸热反应)并达平衡后,仅改变表中反应条件x,下列各项中y随x的增大而增大的是bc(填序号).
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时的甲的转化率 |
9. 在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )
在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )
 在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )
在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )| A. | 该反应在0~t1时间段的速率为:ν(W)=0.25/t1 mol•L-1•min-1 | |
| B. | 反应方程式中的a不可能等于1 | |
| C. | t2时刻改变的条件是通入少量气体Z | |
| D. | t3时刻改变的条件是移去少量物质W |
8.下列选项中,离子方程式书写正确的是( )
| A. | 加入NaClO将污水中的NH3氧化成N2:3ClO-+2NH3=N2↑+3Cl-+3H2O | |
| B. | 泡沫灭火器的灭火原理:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑ | |
| C. | “84消毒液”和“洁厕灵”(主要成分为盐酸)混合使用会产生有毒气体:ClO3-+5Cl-+6H+=3Cl2↑+3H2O | |
| D. | 用足量的氨水吸收硫酸工业尾气中的SO2:SO2+NH3•H2O=NH4++HSO3- |
7.用下列实验装置进行的实验中,能达到相应实验目的是( )


| A. | 用装置甲制取氯气 | |
| B. | 用装置乙干燥氨气 | |
| C. | 用装置丙除去甲烷中混有的乙烯 | |
| D. | 利用装置丁制取硫酸和氢氧化钠,其中b为阴离子交换膜、c为阳离子交换膜 |
6.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol•L-1的氯化铁溶液中,若Fe3+的数目为 NA,则Cl-的数目为3NA | |
| B. | 常温下,1 mol Fe与足量稀HNO3反应,转移电子的数目为2 NA | |
| C. | 8.0gCu2S和CuO的混合物中含有的铜原子数为0.1NA | |
| D. | 标准状况下,2.24 LCl2溶于水,转移电子的数目为0.1NA |
5.下列说法正确的是( )
| A. | 环己醇分子中所有的原子可能共平面 | |
| B. | 按系统命名法,(CH3CH2)2CHCH3化合物的名称是3-乙基丁烷 | |
| C. | 芳香化合物A(C8H8O3)分子中含有酯基和醚键两种含氧官能团,A可能的同分异构体有4种 | |
| D. | 在一定条件下,1.0 mol的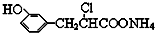 最多能与含4.0 mol NaOH的溶液完全反应 最多能与含4.0 mol NaOH的溶液完全反应 |
4.下列说法正确的是( )
0 156040 156048 156054 156058 156064 156066 156070 156076 156078 156084 156090 156094 156096 156100 156106 156108 156114 156118 156120 156124 156126 156130 156132 156134 156135 156136 156138 156139 156140 156142 156144 156148 156150 156154 156156 156160 156166 156168 156174 156178 156180 156184 156190 156196 156198 156204 156208 156210 156216 156220 156226 156234 203614
| A. | 相同条件下,测得Na2CO3溶液的pH大于相同物质的量浓度的Na2SO3溶液,说明非金属性:C<S | |
| B. | 绝热容器中,向50 mL 1 mol•L-1的盐酸中加入烧碱,水的KW不变 | |
| C. | 相同温度时,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 | |
| D. | 有HX和HY两种弱酸且酸性HX>HY,则物质的量浓度相同的NaX和NaY两溶液等体积混合的溶液中有 c(X-)>c(Y-)>c(OH-)>c(H+) |
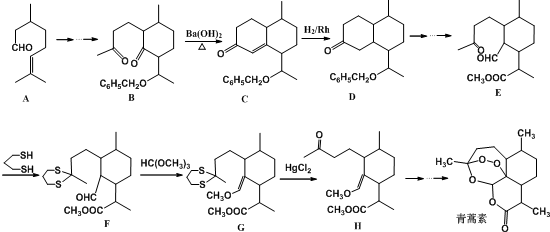
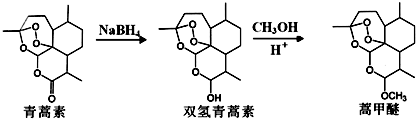
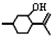 ,则异蒲勒醇分子有3个手性碳原子(连有四种不同原子或原子团的碳原子称为手性碳原子).异蒲勒醇可通过两步反应生成
,则异蒲勒醇分子有3个手性碳原子(连有四种不同原子或原子团的碳原子称为手性碳原子).异蒲勒醇可通过两步反应生成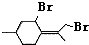 ,请写出相关化学反应方程式
,请写出相关化学反应方程式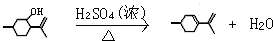 ,
,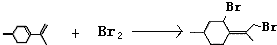 .
.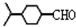 .(填结构简式)
.(填结构简式)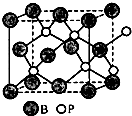 X、Y、Z、W、A五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,A原子的最外层电子数是最内层电子数的一半,其d轨道处于全充满状态.
X、Y、Z、W、A五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,A原子的最外层电子数是最内层电子数的一半,其d轨道处于全充满状态.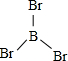 .
.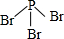 .
.