3.甲苯(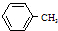 )分子中苯环上的一个氢被-C4H9原子团取代形成的有机物共有( )
)分子中苯环上的一个氢被-C4H9原子团取代形成的有机物共有( )
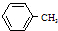 )分子中苯环上的一个氢被-C4H9原子团取代形成的有机物共有( )
)分子中苯环上的一个氢被-C4H9原子团取代形成的有机物共有( )| A. | 8种 | B. | 12种 | C. | 10种 | D. | 16种 |
2.下列说法符合化学事实的是( )
| A. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| B. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 | |
| C. | Na2SiO3水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| D. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 |
1. 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
I.制备
称取14.0g CuSOd•5H20、16.0g Na2CO3.10H20,用研钵分别研细后再混合研磨,立即发生反应,有“滋滋”声,而且混合物很快成为“黏胶状”.将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含SO42-为止,取出沉淀,风干,得到蓝绿色晶体.
(1)①混合物发生反应时有“滋滋”声的原因是有气体生成.
②检验生成物已洗涤干净的方法是取最后一次洗涤液少许于试管中,加入适量盐酸酸化后滴加氯化钡溶液,若无沉淀生成,则没有SO42-,否则含有SO42-
Ⅱ.组成测定
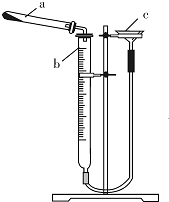
有同学查阅资料发现用Cu(OH)2.CuC03表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2.nCuC03,不同来源的碱式碳酸铜的m、n值需要具体测定.热分解法测定碱式碳酸铜组成的实验装置如图所示.通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值.
(2)①仪器b的名称是碱式滴定管.
②检查装置气密性的方法是连接好装置,通过漏斗向装置中加水,至右侧水面比左侧水面高,静置,水面高度差不发生变化,则装置不 漏气,否则装置漏气.
③三次平行实验测定结果如下表,则该样品中m:n=3:2,若量气管中所盛液体为水,则该测定值比理论值偏大(填“偏大”、“偏小”或“不变”).
III.铜是生命必需的元素,也是人类广泛使用的金属.
(1)将SO2气体通入CuCl2溶液中,生成CuCl沉淀的同时,还有产物H2SO4 HCl(填写化学式).
(2)现代工业上,主要采用高温冶炼黄铜矿(CuFeS2,也可表示为Cu2S•Fe2S3)的方法获得铜.火法炼铜首先要焙烧黄铜矿:2CuFeS2+4O2 $\frac{\underline{\;800℃\;}}{\;}$Cu2S+3SO2+2FeO,每转移0.6mol电子,有0.1mol硫被氧化.
(3)Cu2O投入足量的某浓度的硝酸中,若所得气体产物为NO和NO2的混合物,且体积比为1﹕1,发生反应的化学方程式为:2Cu2O+10HNO3=4Cu(NO3)2+NO↑+NO2↑+5H2O.
 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.I.制备
称取14.0g CuSOd•5H20、16.0g Na2CO3.10H20,用研钵分别研细后再混合研磨,立即发生反应,有“滋滋”声,而且混合物很快成为“黏胶状”.将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含SO42-为止,取出沉淀,风干,得到蓝绿色晶体.
(1)①混合物发生反应时有“滋滋”声的原因是有气体生成.
②检验生成物已洗涤干净的方法是取最后一次洗涤液少许于试管中,加入适量盐酸酸化后滴加氯化钡溶液,若无沉淀生成,则没有SO42-,否则含有SO42-
Ⅱ.组成测定
有同学查阅资料发现用Cu(OH)2.CuC03表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2.nCuC03,不同来源的碱式碳酸铜的m、n值需要具体测定.热分解法测定碱式碳酸铜组成的实验装置如图所示.通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值.
(2)①仪器b的名称是碱式滴定管.
②检查装置气密性的方法是连接好装置,通过漏斗向装置中加水,至右侧水面比左侧水面高,静置,水面高度差不发生变化,则装置不 漏气,否则装置漏气.
③三次平行实验测定结果如下表,则该样品中m:n=3:2,若量气管中所盛液体为水,则该测定值比理论值偏大(填“偏大”、“偏小”或“不变”).
| 实验序号 | 样品质量/g | CO2体积/mL(已折算成标准状况下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
(1)将SO2气体通入CuCl2溶液中,生成CuCl沉淀的同时,还有产物H2SO4 HCl(填写化学式).
(2)现代工业上,主要采用高温冶炼黄铜矿(CuFeS2,也可表示为Cu2S•Fe2S3)的方法获得铜.火法炼铜首先要焙烧黄铜矿:2CuFeS2+4O2 $\frac{\underline{\;800℃\;}}{\;}$Cu2S+3SO2+2FeO,每转移0.6mol电子,有0.1mol硫被氧化.
(3)Cu2O投入足量的某浓度的硝酸中,若所得气体产物为NO和NO2的混合物,且体积比为1﹕1,发生反应的化学方程式为:2Cu2O+10HNO3=4Cu(NO3)2+NO↑+NO2↑+5H2O.
20.有关下图及实验的描述正确的是( )
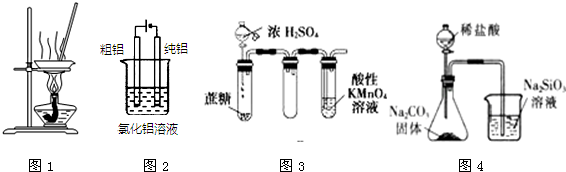

| A. | 用图1装置蒸发FeCl3溶液制备无水FeCl3 | |
| B. | 用图2装置精炼铝 | |
| C. | 用图3装置证明浓硫酸具有脱水性和强氧化性 | |
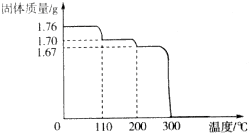
| D. | 用图4装置可比较氯、碳、硅三种元素的非金属性强弱 |
19.室温下,关于下列溶液的说法正确的是( )


| A. | 25℃时①10-3mol/L的盐酸;②pH=3的NH4Cl溶液;③pH=11的氨水中,水的电离程度为:②>③>① | |
| B. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| C. | pH=8.0的KHS溶液中,c(K+)>c(HS-)>c(OH-)>c(S2-)>c(H+) | |
| D. | 图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+c(CH3COOH) |
18.下列说法正确的是( )
| A. | 乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的 | |
| B. | 棉、丝、羽毛、塑料及合成橡胶完全燃烧都只生成CO2和H2O | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 新型材料聚酯纤维、光导纤维都属于有机高分子化合物 |
15.下列实验不能达到预期目的是( )
| A. | 用稀硫酸和锌粒反应制取氢气时加入少许硫酸铜粉末以加快反应速率 | |
| B. | 向乙酸乙酯中加入饱和碳酸钠溶液以除去乙酸乙酯中少量的乙酸 | |
| C. | 向盛有沸水的烧杯中滴加FeC13饱和溶液并长时间煮沸以制取Fe(OH)3胶体 | |
| D. | 向蔗糖中滴加浓硫酸可证明浓硫酸有脱水性 |
14.EPA、DHA均为不饱和羧酸.1mol分子式为C67H96O6的某种鱼油完全水解后生成1mol 甘油(C3H8O3),1mol EPA和2mol DHA,EPA,DHA的分子式分别为( )
0 156031 156039 156045 156049 156055 156057 156061 156067 156069 156075 156081 156085 156087 156091 156097 156099 156105 156109 156111 156115 156117 156121 156123 156125 156126 156127 156129 156130 156131 156133 156135 156139 156141 156145 156147 156151 156157 156159 156165 156169 156171 156175 156181 156187 156189 156195 156199 156201 156207 156211 156217 156225 203614
| A. | C20H30O2、C22H30O2 | B. | C22H32O2、C20H30O2 | ||
| C. | C22H30O2、C20H30O2 | D. | C20H30O2、C22H32O2 |
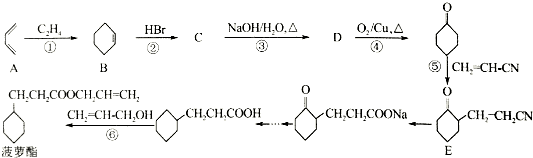
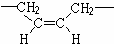 ,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.
,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.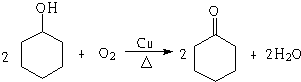 .
.
 .
.