3.下列有关“化学与生活、社会”的叙述正确的是( )
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 屠呦呦获得了2015年诺贝尔奖,她用乙醚提取青蒿素的过程属于化学变化 |
1.根据如图海水综合利用的工业流程图,判断下列说法正确的是( )
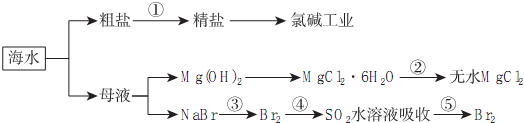

| A. | 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程④中SO2被氧化 | |
| C. | 从第③步到第⑤步的目的是为了浓缩 | |
| D. | 从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
20.N2的结构可以表示为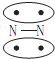 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是 ( )
,其中椭圆框表示π键,下列说法中不正确的是 ( )
 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是 ( )
,其中椭圆框表示π键,下列说法中不正确的是 ( )| A. | N2分子与CO分子中都含有叁键 | |
| B. | CO分子中有一个π键是配位键 | |
| C. | N2、CO分别由非极性键和极性键结合,因此二者不是等电子体 | |
| D. | N2与CO的化学性质相同 |
17.短周期主族元素X、Y、Z、W原子序数依次增大,X-与氦原子电子层结构相同,Y原子核外L层电子数为8且Y与X同主族,Z原子的最外层电子数是内层电子总数的一半,W的最高正价与最低负价的代数和为4,下列说法正确的是( )
| A. | X、Y间可形成离子化合物 | |
| B. | 单质熔点:Y>W>X | |
| C. | 最高价氧化物对应水化物的酸性:Z>W | |
| D. | Y、W形成的单核离子均能破坏水的电离平衡 |
16.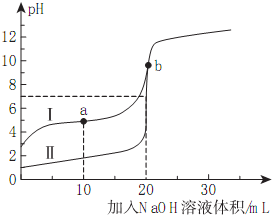 室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )
室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )
 室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )
室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )| A. | 当Ⅰ代表HB,b点时体系中有:c(B-)+c(HB)=0.05mol/L | |
| B. | 滴定分析中,甲基橙不能用做滴定曲线Ⅰ中的指示剂 | |
| C. | a点时的溶液中离子浓度最大的是c(Na+) | |
| D. | 若Ⅱ代表HA的滴定曲线,则Ka(HB)≈10-5 |
15.铜的冶炼大致可分为:
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2↑;
④电解精炼铜.
下列说法不正确( )
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2↑;
④电解精炼铜.
下列说法不正确( )
| A. | 上述灼烧过程的尾气回收后可用来制硫酸 | |
| B. | 上述过程中,由6molCuFeS2制取6molCu时共消耗15molO2 | |
| C. | 在反应2Cu2O+Cu2S=6Cu+SO2↑中,氧化产物与还原产物的物质的量比1:6 | |
| D. | 在反应2Cu2O+Cu2S=6Cu+SO2↑中,只有Cu2O作氧化剂 |
14.下列有关实验装置、操作,不能实现相应实验目的是( )
0 156029 156037 156043 156047 156053 156055 156059 156065 156067 156073 156079 156083 156085 156089 156095 156097 156103 156107 156109 156113 156115 156119 156121 156123 156124 156125 156127 156128 156129 156131 156133 156137 156139 156143 156145 156149 156155 156157 156163 156167 156169 156173 156179 156185 156187 156193 156197 156199 156205 156209 156215 156223 203614
| A | B | C | D | |
| 装置 | 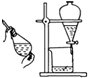 | 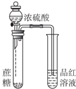 | 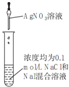 | 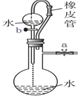 |
| 目的 | 用NaOH溶液除去溴苯中单质溴 | 证明浓硫酸有脱水性、强氧化性 | 确定Ksp(AgCl)、Ksp(AgI)的相对大小 | 观察水能否全部流下判断装置气密性 |
| A. | A | B. | B | C. | C | D. | D |
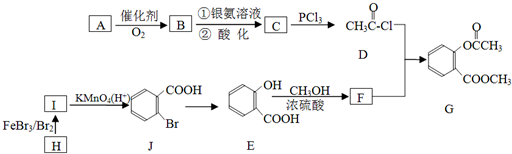
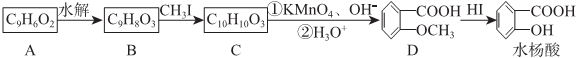
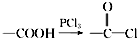 ,请回答以下问题:
,请回答以下问题: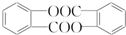 .
.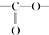 结构
结构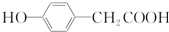 .
.
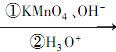 RCOOH+R1COOH
RCOOH+R1COOH .
.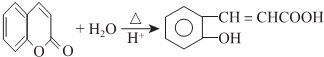 .
.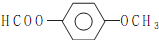 .
.