12.某均匀混合的白色粉末可能含有下列7种常见物质中的某4种:NaCl、BaCl2、Mg(NO3)2、K2CO3、CuSO4、NaHCO3、X,混合物中各成分的物质的量相等,且所含阴、阳离子数目之比为3:2,某同学做了以下实验,部分现象没有描述.根据所提供的实验现象,下列对该白色粉末的判断正确的是( )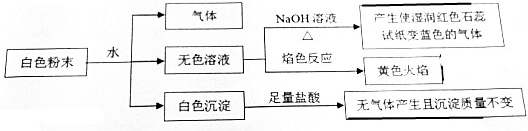

| A. | 一定含有BaCl2、Mg(NO3)2、NaHCO3、X,且X是NH4HSO4 | |
| B. | 一定不含K2CO3、CuSO4,X是NH4Al(SO4)2 | |
| C. | 一定含有BaCl2、NaHCO3、X且X是NH4AlO2,另一种为NaCl和Mg(NO3)2中的任一种 | |
| D. | 一定含有NaCl、BaCl2、NaHCO3和X,当X不能确定是什么物质 |
11.某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查) 请回答:
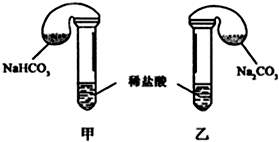
(1)各组反应开始时,甲装置中的气球体积先变大,该装置中反应的离子方程式是HCO3-+H+=CO2↑+H2O.
(2)当试管中不再有气体生成时,两组实验出现不同现象,填写下表的空格.

(1)各组反应开始时,甲装置中的气球体积先变大,该装置中反应的离子方程式是HCO3-+H+=CO2↑+H2O.
(2)当试管中不再有气体生成时,两组实验出现不同现象,填写下表的空格.
| 试剂用量 | 实验现象 (气球体积变化) | 分析原因 | |
| 第 ① 组 | 42g NaHCO3 53g Na2CO3 300mL4mol/L盐酸 | 甲中气球与乙中 气球的体积相等 | 甲、乙盐酸均过量 n(NaHCO3)=n (Na2CO3) V甲(CO2)=V乙(CO2) |
| 第 ② 组 | 42g NaHCO3 53g Na2CO3 300mL3mol/L盐酸 | 甲中气球体积大于乙中气球的体积(填“大于”或“小于” 或“等于”) |
10.除去下列括号内杂质的试剂或方法错误的是( )
| A. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| B. | Fe2+(Fe3+),还原铁粉,过滤 | |
| C. | Cl2(HCl),饱和食盐水,洗气 | |
| D. | CO2(SO2),饱和NaHCO3溶液、浓硫酸,洗气 |
8. 碘在科研与生活中有重要应用,某兴趣小组用0.50mol•L-1 KI、0.2%淀粉溶液、0.20mol•L-1 K2S2O8、0.10mol•L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
碘在科研与生活中有重要应用,某兴趣小组用0.50mol•L-1 KI、0.2%淀粉溶液、0.20mol•L-1 K2S2O8、0.10mol•L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
已知:S2O82-+2I-═2SO42-+I2(慢) I2+2S2O32-═2I-+S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-):n(S2O82-)<2.
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx2.0 mL,理由是保证反应物K2S2O8浓度改变,而其他的条件不变,才能达到实验目的.
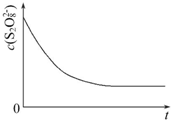
(3)已知某条件下,浓度c(S2O82-)反应时间t的变化曲线如图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)-t的变化曲线示意图(进行相应的标注)
(4)碘也可用作心脏起搏器电源-锂碘电池的材料,该电池反应为:
2Li(s)+I2(s)═2LiI(s)△H
已知:①4Li(s)+O2(g)═2Li2O(s)△H1
②4LiI(s)+O2(g)═2I2(s)+2Li2O(s)△H2
则电池反应的△H=$\frac{△{H}_{1}-△{H}_{2}}{2}$;碘电极作为该电池的正极.
 碘在科研与生活中有重要应用,某兴趣小组用0.50mol•L-1 KI、0.2%淀粉溶液、0.20mol•L-1 K2S2O8、0.10mol•L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
碘在科研与生活中有重要应用,某兴趣小组用0.50mol•L-1 KI、0.2%淀粉溶液、0.20mol•L-1 K2S2O8、0.10mol•L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响.已知:S2O82-+2I-═2SO42-+I2(慢) I2+2S2O32-═2I-+S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-):n(S2O82-)<2.
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
(3)已知某条件下,浓度c(S2O82-)反应时间t的变化曲线如图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)-t的变化曲线示意图(进行相应的标注)
(4)碘也可用作心脏起搏器电源-锂碘电池的材料,该电池反应为:
2Li(s)+I2(s)═2LiI(s)△H
已知:①4Li(s)+O2(g)═2Li2O(s)△H1
②4LiI(s)+O2(g)═2I2(s)+2Li2O(s)△H2
则电池反应的△H=$\frac{△{H}_{1}-△{H}_{2}}{2}$;碘电极作为该电池的正极.
7.下列实验操作不会引起误差的是( )
| A. | 酸碱中和滴定时,用待测液润洗锥形瓶 | |
| B. | 酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液 | |
| C. | 用NaOH标准溶液测定未知浓度的盐酸溶液时,锥形瓶使用前中含有少量水 | |
| D. | 用标准盐酸测定未知浓度NaOH溶液,结束实验时,酸式滴定管尖嘴部分有气泡,开始实验时无气泡 |
6. 某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
①称取W g样品,准确配成500mL溶液.
②准确配制0.1000mol/L的标准盐酸.
③用滴定管取所配制碱液25.00mL于锥形瓶,并向瓶中滴几滴甲基橙试液.
④向锥形瓶中逐滴滴入标准盐酸,直到终点.
⑤记录数据,计算.请回答:
(1)在①操作中要使用的定量的玻璃仪器是500ml容量瓶.
(2)操作④装标准盐酸的滴定管是酸式滴定管.
(3)滴定过程中左手控制酸式滴定管的活塞,右手向一个方向摇动锥形瓶.眼睛应始终注视锥形瓶内溶液的颜色变化,判断滴定到达终点的现象是滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
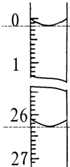
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为26.10ml.
(5)某学生根据3次实验分别记录有关数据如表:
②依据上表数据列式计算该NaOH溶液的物质的量浓度(计算结果取4位有效数).
③根据上面结果计算NaOH的纯度$\frac{2.096}{W}$×100%.
(6)下列操作中,可能使测定结果偏低的是ACF.
A.称取样品时,样品和砝码位置放反了
B.配制标准盐酸过程中,读取量筒读数时,俯视刻度线
C.碱式滴定管清洗后,未用待测液润洗
D.酸式滴定管清洗后,未用待测液润洗
E.锥形瓶装液前未干燥,有水珠附着在瓶壁
F.读取酸式滴定管读数时,第一次读数仰视,第二次读数俯视.
 某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:①称取W g样品,准确配成500mL溶液.
②准确配制0.1000mol/L的标准盐酸.
③用滴定管取所配制碱液25.00mL于锥形瓶,并向瓶中滴几滴甲基橙试液.
④向锥形瓶中逐滴滴入标准盐酸,直到终点.
⑤记录数据,计算.请回答:
(1)在①操作中要使用的定量的玻璃仪器是500ml容量瓶.
(2)操作④装标准盐酸的滴定管是酸式滴定管.
(3)滴定过程中左手控制酸式滴定管的活塞,右手向一个方向摇动锥形瓶.眼睛应始终注视锥形瓶内溶液的颜色变化,判断滴定到达终点的现象是滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为26.10ml.
(5)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V=26.20 |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.45 | |
③根据上面结果计算NaOH的纯度$\frac{2.096}{W}$×100%.
(6)下列操作中,可能使测定结果偏低的是ACF.
A.称取样品时,样品和砝码位置放反了
B.配制标准盐酸过程中,读取量筒读数时,俯视刻度线
C.碱式滴定管清洗后,未用待测液润洗
D.酸式滴定管清洗后,未用待测液润洗
E.锥形瓶装液前未干燥,有水珠附着在瓶壁
F.读取酸式滴定管读数时,第一次读数仰视,第二次读数俯视.
5.《化学反应原理》一书中,我们学习了两个重要的定量实验.请回答下列问题:
Ⅰ、某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q(放)=C m(t2-t1),反应后溶液的比热容C为4.18KJ?℃-1?Kg-1,m指溶液的质量,各物质的密度均为1g?cm-3.
①计算分析△H=-56.8KJ/mol.(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8KJ/mol.
Ⅱ、为了测定含有H2C2O4•2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为c(HC2O4-)>c(C2O42-)>c(H2C2O4).
(2)完成并配平下列离子方程式
5C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
(3)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4•2H2O的质量分数偏小.(填“偏大”、“偏小”或“无影响”)
(4)步骤③中判断滴定终点的方法是滴入最后一滴溶液呈紫红色且半分钟颜色不变.
(5)常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
(i)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-,HC2O4-?H++C2O42-.
(ii)KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题)HC2O4-?H++C2O42-,HC2O4-+H2O?H2C2O4+OH-,但其电离程度大于水解程.
(iii)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42- ) b.c(Na+)═c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42- ) d.c(K+)>c(Na+)
Ⅰ、某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实 验 试剂如下: | 溶 液 温 度 | 中和热△H | ||||
| t1 | t2 | |||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | ||
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | ||
①计算分析△H=-56.8KJ/mol.(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8KJ/mol.
Ⅱ、为了测定含有H2C2O4•2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为c(HC2O4-)>c(C2O42-)>c(H2C2O4).
(2)完成并配平下列离子方程式
5C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
(3)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4•2H2O的质量分数偏小.(填“偏大”、“偏小”或“无影响”)
(4)步骤③中判断滴定终点的方法是滴入最后一滴溶液呈紫红色且半分钟颜色不变.
(5)常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(ii)KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题)HC2O4-?H++C2O42-,HC2O4-+H2O?H2C2O4+OH-,但其电离程度大于水解程.
(iii)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42- ) b.c(Na+)═c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42- ) d.c(K+)>c(Na+)
4.自来水中游离氯的测定.设计如下实验:取一定量自来水置于锥形瓶中,加入足量的KI溶液及2~3滴指示剂,用0.0010mol•L-1的Na2S2O3溶液滴定反应中生成的I2(I2被还原为I-,S2O32-被氧化为S4O62-),根据消耗的Na2S2O3溶液的体积计算出自来水中游离氯的浓度.请回答下列问题:
(1)写出Na2S2O3与I2反应的离子方程式I2+2S2O32-=2I-+S4O62-.
(2)滴定中使用的指示剂是淀粉溶液,滴定终点的现象是蓝色溶液恰好变为无色且半分钟内不恢复.
(3)该小组同学的实验数据如下表:
请根据上表数据计算该自来水中游离氯(Cl2)的物质的量浓度.0.0010mol•L-1(写出计算过程,否则不得分)
(4)若实验中的锥形瓶用自来水洗净后未用蒸馏水洗涤,则实验值大于(填“大于、小于或等于”)实际值.
0 156024 156032 156038 156042 156048 156050 156054 156060 156062 156068 156074 156078 156080 156084 156090 156092 156098 156102 156104 156108 156110 156114 156116 156118 156119 156120 156122 156123 156124 156126 156128 156132 156134 156138 156140 156144 156150 156152 156158 156162 156164 156168 156174 156180 156182 156188 156192 156194 156200 156204 156210 156218 203614
(1)写出Na2S2O3与I2反应的离子方程式I2+2S2O32-=2I-+S4O62-.
(2)滴定中使用的指示剂是淀粉溶液,滴定终点的现象是蓝色溶液恰好变为无色且半分钟内不恢复.
(3)该小组同学的实验数据如下表:
| 实验序号 | 自来水的体积 | KI溶液的体积 | 消耗的Na2S2O3溶液的体积 |
| 1 | 10.00mL | 10.00mL | 19.96mL |
| 2 | 10.00mL | 10.00mL | 20.04mL |
(4)若实验中的锥形瓶用自来水洗净后未用蒸馏水洗涤,则实验值大于(填“大于、小于或等于”)实际值.

