10.短周期元素X、Y、Z、W在元素周期表中的位置如图所示,若W原子最外层电子数是其内层电子总数的$\frac{3}{5}$.下列说法中,正确的是( )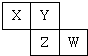

| A. | 元素X是自然界中形成化合物种类最多的元素 | |
| B. | 气态氢化物的稳定性Z>W>Y | |
| C. | 原子半径由大到小排列顺序Z>Y>X | |
| D. | W只有一种氧化物 |
9.W、X、Y、Z是1-20号元素中的四种元素,原子序数依次增大;W的主要化合价为-2价,原子半径为0.074nm,X所在的主族序数与所在的周期序数之差为3;Y原子最外层电子数为奇数;Z最高价氧化物对应的水化物电离出的阴、阳离子数目相等,下列说法正确的是( )
| A. | W可能是氧元素,也可能是硫元素 | |
| B. | X元素氧化物对应的水化物一定是一种强酸 | |
| C. | Y元素原子次外层电子数与最外层电子敦之差为1 | |
| D. | Z可能是氯元素,也可能是钾元素 |
6.下列有关化学实验仪器的使用方法及操作正确的是( )
| A. | 用规格为100mL的量筒量取89.7mL蒸馏水 | |
| B. | 用容量瓶配制一定物质的量浓度的溶液前需用标准液润洗 | |
| C. | 打开分液漏斗、长颈漏斗、滴液漏斗的活塞,均可放出其中液体 | |
| D. | 锥形瓶、烧杯、烧瓶均可垫加石棉网加热 |
4.已知25℃时,有关弱酸的电离平衡常数:
则下列有关说法不正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
| A. | NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)-c(OH-)=c(HCO3-)+2c(CO32-) | |
| B. | 25℃时,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 | |
| C. | 25℃时,若同浓度的醋酸和氢氧化钠等体积混合,所得溶液pH=8,则 c(Na+)-c(CH3COO-)=9.9×10-7mol/L | |
| D. | 25℃时,0.1mol/L的各溶液的pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
3.短周期元素X、Y、Z、W、R的化合价与原子序数的关系如下图所示.下列说法正确的是( )


| A. | 离子半径:W3+>Z+>Y2- | |
| B. | X、Y都存在同素异形现象 | |
| C. | Z和Y形成的化合物中只存在离子键 | |
| D. | 常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液 |
2.下列有关物质的性质和应用都正确的是( )
| A. | BaSO4的水溶液不导电,故BaSO4是弱电解质 | |
| B. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也不存在同分异构体 | |
| C. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| D. | AgCl在同温、同浓度的CaCl2和NaCl溶液中的溶解度不同 |
1.化学与生产、生活、社会密切相关,下列有关说法中正确的是( )
0 156020 156028 156034 156038 156044 156046 156050 156056 156058 156064 156070 156074 156076 156080 156086 156088 156094 156098 156100 156104 156106 156110 156112 156114 156115 156116 156118 156119 156120 156122 156124 156128 156130 156134 156136 156140 156146 156148 156154 156158 156160 156164 156170 156176 156178 156184 156188 156190 156196 156200 156206 156214 203614
| A. | 苯酚有一定毒性,不能作消毒剂和防腐剂 | |
| B. | 纤维素可水解成葡萄糖,人类可从中获得生存所需的能量 | |
| C. | 2014年1月,国家首次将雾霾天气纳入自然灾情进行通报,雾霾是一种不同于胶体的分散系,它的形成与大量焚烧田间秸秆有关 | |
| D. | 煤经气化和液化两个物理变化过程,可变为清洁能源 |
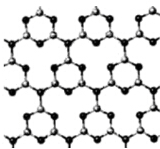
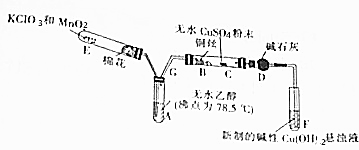
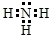 ;由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X中所含化学键类型极性键、非极性键;(填写“极性共价键”、“非极性共价键”、“离子键”)向X中加入酸性KMnO4溶液,写出二者恰好反应的离子方程式5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8H2O;
;由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X中所含化学键类型极性键、非极性键;(填写“极性共价键”、“非极性共价键”、“离子键”)向X中加入酸性KMnO4溶液,写出二者恰好反应的离子方程式5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8H2O;