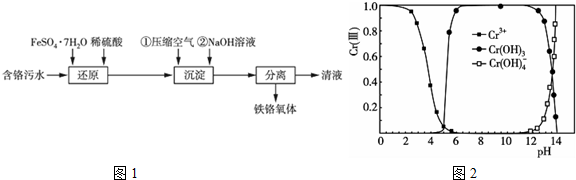
8.化学在环境保护中起着十分重要的作用,电化学降解MO3-的原理如图所示:则下列判断正确的是


| A. | 电源正极为B | |
| B. | 若电解过程中转移了1mol电子,则膜两侧电解液的质量变化差(|△m左|-|△m右|)为7.2克 | |
| C. | Pt电极上产物为H2 | |
| D. | Ag-Pt电极上发生氧化反应 |
7.A、B、C、D、E五种元素分属于三个短周期,且原子序数依次增大.A、C同主族,可形成离子化合物CA;B、D同主族,且D的原子序数是B的2倍,则下列说法正确的是( )
| A. | B元素在周期表中的位置为第二周期ⅣA族 | |
| B. | D的氧化物和E的单质的水溶液均有漂白性,且漂白的原理相同 | |
| C. | 由A、B、C、D组成的两种盐的溶液反应可产生DB2气体 | |
| D. | 上述元素的非金属气态氢化物还原性最强的是E |
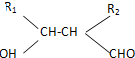
6.尿黑酸是苯丙氨酸和酪氨酸的中间产物,其结构简式为 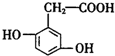 ,则下列说法错误的是( )
,则下列说法错误的是( )
 ,则下列说法错误的是( )
,则下列说法错误的是( )| A. | 1mol尿黑酸与足量的浓溴水反应,最多消耗3mol Br2 | |
| B. | 1mol尿黑酸最多能与4mol H2反应 | |
| C. | 尿黑酸分子中在同一平面上的碳原子至少有7个 | |
| D. | 尿黑酸可与碳酸氢钠溶液反应放出CO2,生成2.24LCO2(标况下)需要尿黑酸16.8g |
5.下列关于化学反应的描述正确的是( )
| A. | 铵明矾中加入过量的氢氧化钡溶液的离子方程式为Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| B. | 2Cu(IO3)2+24KI+12H2SO4═2CuI↓+13I2+12K2SO4+12H2O中,当1mol氧化剂参加反应时,被氧化的物质的物质的量为11mol | |
| C. | 强碱溶液中,用次氯酸钠与Fe(OH)2反应是湿法制备高铁酸钠的最主要过程,可表示为:3ClO-+2Fe(OH)2═2FeO42-+3Cl-+H2O+4H+ | |
| D. | 将过量SO2通入少量氨水中的离子方程式为:SO2+2NH3•H2O═2NH4++SO32- |
4.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 42g丙烯和环丙烷的混合气体中所含极性键的数目为9NA | |
| B. | 12g石墨烯(单层石墨)中含有六元环的数目为0.5NA | |
| C. | 室温下,1L pH=13的NaOH溶液中,由水电离出的OH-的数目为0.1NA | |
| D. | 3.6 g CaO2晶体中阴离子的数目为0.1NA |
3.化学与人类的生活、生产息息相关,下列说法正确的是( )
0 156016 156024 156030 156034 156040 156042 156046 156052 156054 156060 156066 156070 156072 156076 156082 156084 156090 156094 156096 156100 156102 156106 156108 156110 156111 156112 156114 156115 156116 156118 156120 156124 156126 156130 156132 156136 156142 156144 156150 156154 156156 156160 156166 156172 156174 156180 156184 156186 156192 156196 156202 156210 203614
| A. | BaSO4在医学上用作“钡餐”,Ba2+对人体无害 | |
| B. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性 | |
| C. | 光导纤维的主要成分是单质硅,太阳能电池使用的材料是SiO2 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂或燃油 |
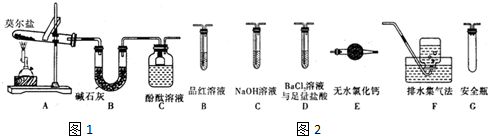
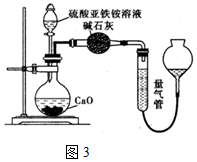
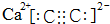 .
.
 .
.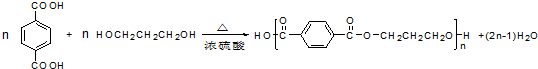 .
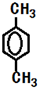
.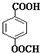 (填结构简式).
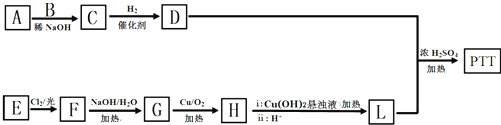
(填结构简式).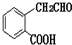 和CH3OH为有机原料制备化合物
和CH3OH为有机原料制备化合物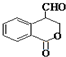 的合成路线流程图(无机试剂任选).(合成路线流程图示例如下CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2$\stackrel{Br_{2}}{→}$
的合成路线流程图(无机试剂任选).(合成路线流程图示例如下CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2$\stackrel{Br_{2}}{→}$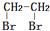 )
)