10.下列反应的离子方程式正确的是( )
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+=Cu2++2H2O | |
| C. | NaHCO3溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+H2O+CO32- | |
| D. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
9.下列粒子半径最小的是( )
| A. | Na+ | B. | Mg2+ | C. | S2- | D. | Cl- |
6.根据有机化合物的系统命名法,下列命名正确的是( )
| A. | 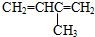 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. |  2-羟基丁烷 2-羟基丁烷 | ||
| C. |  2-乙基丁烷 2-乙基丁烷 | D. |  邻羟基苯甲酸 邻羟基苯甲酸 |
4.下表为部分短周期主族元素的相关信息.
请回答下列问题:
(1)Z元素在周期表中的位置是第三周期第ⅦA族.
(2)元素T与X按原子个数比1:1形成的化合物B所含的化学键有离子键、共价键(填化学键名称).
(3)已知1mol化合物A与Na2SO3在溶液中发生反应时,转移2mol电子,写出该反应的离子方程式SO32-+ClO-═SO42-+Cl-.
| 元素 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子内层电子数是其最外层电子数的三分之一 |
| Y | 在第三周期元素中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
(1)Z元素在周期表中的位置是第三周期第ⅦA族.
(2)元素T与X按原子个数比1:1形成的化合物B所含的化学键有离子键、共价键(填化学键名称).
(3)已知1mol化合物A与Na2SO3在溶液中发生反应时,转移2mol电子,写出该反应的离子方程式SO32-+ClO-═SO42-+Cl-.
3.表是部分元素在周期表的位置,表中列有①~⑩中元素,用元素符号或化学式填空回答
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为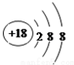
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(3)写出⑤的最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(4)某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L.则HXR的相对分子量为34;HXR的化学式为H2S.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;
(3)写出⑤的最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(4)某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L.则HXR的相对分子量为34;HXR的化学式为H2S.
2.已知X、Y、Z、R均为短周期元素,其中X与R为同族元素,且X的元素原子序数是R原子序数的2倍,X、Y处于同一周期,Y的原子半径是本周期元素原子中最大的,Z元素是所有元素中非金属性最强的元素.下列说法不正确的是( )
0 156002 156010 156016 156020 156026 156028 156032 156038 156040 156046 156052 156056 156058 156062 156068 156070 156076 156080 156082 156086 156088 156092 156094 156096 156097 156098 156100 156101 156102 156104 156106 156110 156112 156116 156118 156122 156128 156130 156136 156140 156142 156146 156152 156158 156160 156166 156170 156172 156178 156182 156188 156196 203614
| A. | 原子最外层电子数:Z>X=R>Y | |
| B. | Z与R形成的化合物中R显正价 | |
| C. | 离子半径:X2->Y+>R2->Z- | |
| D. | 四种元素中X元素形成的氢化物沸点最低 |


 .
.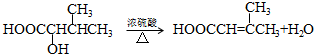 .
. .
. .
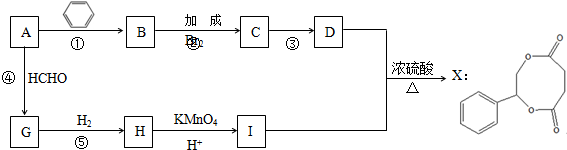
.
 .
. .
. .
. 任意2种.
任意2种. .
.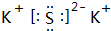 ;
;