16.元素的下列性质按C、N、O、F顺序递增的是( )
| A. | 最高正化合价 | B. | 非金属性 | C. | 电子层数 | D. | 原子半径 |
13.X、Y、M、N四种相邻主族短周期元素的相对位置如下表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性.
注意:用化学式回答下列问题(不要以字母代替)
(1)元素Y在周期表中的位置是第三周期第ⅢA族,其单质可采用电解熔融Al2O3的方法制备.
(2)M、N、Y三种元素最高价氧化物的水化物中,酸性最强的是HNO3,将过量的N形成的最常见氢化物通入到Y的氯化物溶液中,产生的现象是产生白色沉淀.
(3)气体分子(MN)2的电子式为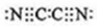 ,(MN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为(CN)2+2NaOH=NaCN+NaCNO+H2O,若还原性MN->I-,将适量的(MN)2、I2、KMN、KI在水中混合后,反应的离子方程式为I2+2CN-=2I-+(CN)2.
,(MN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为(CN)2+2NaOH=NaCN+NaCNO+H2O,若还原性MN->I-,将适量的(MN)2、I2、KMN、KI在水中混合后,反应的离子方程式为I2+2CN-=2I-+(CN)2.
| M | N | ||
| X | Y |
(1)元素Y在周期表中的位置是第三周期第ⅢA族,其单质可采用电解熔融Al2O3的方法制备.
(2)M、N、Y三种元素最高价氧化物的水化物中,酸性最强的是HNO3,将过量的N形成的最常见氢化物通入到Y的氯化物溶液中,产生的现象是产生白色沉淀.
(3)气体分子(MN)2的电子式为
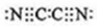 ,(MN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为(CN)2+2NaOH=NaCN+NaCNO+H2O,若还原性MN->I-,将适量的(MN)2、I2、KMN、KI在水中混合后,反应的离子方程式为I2+2CN-=2I-+(CN)2.
,(MN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为(CN)2+2NaOH=NaCN+NaCNO+H2O,若还原性MN->I-,将适量的(MN)2、I2、KMN、KI在水中混合后,反应的离子方程式为I2+2CN-=2I-+(CN)2.
12.依据事实,写出下列反应的热化学方程式或按要求填空
(1)已知:HCN(aq)+NaOH(aq)=NaCN (aq)+H2O(l)△H=-12.1kJ/mol
HCl(aq)+NaOH(aq)=NaCl (aq)+H2O(l)△H=-55.6kJ/mol
写出HCN在水溶液中电离的热化学方程式HCN(aq)=H+(aq)+CN-(aq)△H=+43.5kJ/mol.此空删去
(2)已知CH3-CH3(g)→CH2=CH2(g)+H2(g),有关化学键的键能如表:
试计算该反应的反应热为+125 kJ/mol
(3)在1L的密闭容器中充入1molN2气和3molH2气体,在一定条件下发生反应:一段时间后,测得容器内混合气体的压强是反应前的0.9倍,此时体系放热a KJ,请写出该反应的热化学方程式N2(g)+3H2(g)=2NH3(g)△H=-5akJ/mol.
(1)已知:HCN(aq)+NaOH(aq)=NaCN (aq)+H2O(l)△H=-12.1kJ/mol
HCl(aq)+NaOH(aq)=NaCl (aq)+H2O(l)△H=-55.6kJ/mol
写出HCN在水溶液中电离的热化学方程式HCN(aq)=H+(aq)+CN-(aq)△H=+43.5kJ/mol.此空删去
(2)已知CH3-CH3(g)→CH2=CH2(g)+H2(g),有关化学键的键能如表:
| 化学键 | C-H | C=C | C-C | H-H |
| 键能 (kJ/mol) | 414 | 615 | 347 | 435 |
(3)在1L的密闭容器中充入1molN2气和3molH2气体,在一定条件下发生反应:一段时间后,测得容器内混合气体的压强是反应前的0.9倍,此时体系放热a KJ,请写出该反应的热化学方程式N2(g)+3H2(g)=2NH3(g)△H=-5akJ/mol.
11.有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如表所示:
下列各项判断正确的是( )
| 第一组 | A-268.8 | B-249.5 | C-185.8 | D-151.7 |
| 第二组 | F2-187.0 | Cl2-33.6 | Br2 58.7 | I2 184.0 |
| 第三组 | HF 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | H2Se 42.0 | H2Te-1.8 |
| A. | 第一组和第二组物质中一定含有共价键 | |
| B. | 第三组与第四组相比较,化合物的稳定顺序为:HBr>H2Se | |
| C. | 第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI | |
| D. | 第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强 |
10.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
| A. | 若原子半径X>Y,则气态氢化物稳定性:HmX<HnY | |
| B. | X、Y一定不是同周期元素 | |
| C. | 由mXa-与nYb-得m+a=n-b | |
| D. | Xa-的还原性一定强于Yb- |
9.下列有关性质的比较,不能用元素周期律解释的是( )
①酸性:H2SO4>H3PO4 ②热稳定性:Na2CO3>NaHCO3 ③非金属性:Cl>Br
④熔点:H2O>H2S ⑤碱性:NaOH>NH3•H2O ⑥稳定性:H2O>H2S
⑦酸性:HI>HCl ⑧还原性:HI>HCl.
0 155981 155989 155995 155999 156005 156007 156011 156017 156019 156025 156031 156035 156037 156041 156047 156049 156055 156059 156061 156065 156067 156071 156073 156075 156076 156077 156079 156080 156081 156083 156085 156089 156091 156095 156097 156101 156107 156109 156115 156119 156121 156125 156131 156137 156139 156145 156149 156151 156157 156161 156167 156175 203614
①酸性:H2SO4>H3PO4 ②热稳定性:Na2CO3>NaHCO3 ③非金属性:Cl>Br
④熔点:H2O>H2S ⑤碱性:NaOH>NH3•H2O ⑥稳定性:H2O>H2S
⑦酸性:HI>HCl ⑧还原性:HI>HCl.
| A. | ①③⑥⑧ | B. | ③④⑤⑥ | C. | ②④⑤⑦⑧ | D. | ②④⑤⑦ |
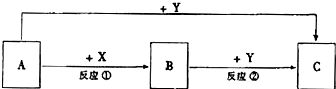
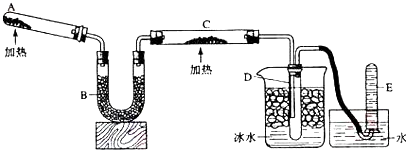
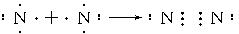 ,Y的分子式为NO,W的结构式为
,Y的分子式为NO,W的结构式为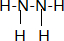 .
.