6.下列属于氧化还原反应的是( )
| A. | 钠与水反应 | B. | FeCl3与NaOH溶液反应 | ||
| C. | Al(OH)3与盐酸反应 | D. | NaHCO3受热分解 |
5.下列各组混合物,能用分液的方法分离的是( )
| A. | 氯化钠和泥沙 | B. | 汽油和柴油 | C. | 四氯化碳和水 | D. | 氯化钙和硫酸钡 |
3.温度为T 时,将0.40mol A气体充入2.0L固定容积的密闭容器中,发生反应A(g)═2B(g);△H>0,经过一段时间后达到平衡.反应过程中测得的部分数据见下表:下列说法正确的是( )
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| n(A)/mol | 0.40 | - | 0.20 | - | - | 0.10 |
| n(B)/mol | 0.00 | 0.24 | - | 0.52 | 0.60 | 0.60 |
| A. | 0~40 s的平均反应速率v(B)=0.01 mol•L-1•s-1 | |
| B. | 80 s时容器中混合气体的密度小于40 s时混合气体的密度 | |
| C. | 其他条件不变,加入合适的催化剂,0~80 s时间段内v(A)>0.001 875 mol•L-1•s-1 | |
| D. | 反应达到最大限度后,增加A的浓度,B的生成速率不变 |
1.有M、X、Y、Z、W五种原子序数依次增大的短周期主族元素,其中M、Z同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法正确的是( )
| A. | X、M两种元素形成的化合物中只能存在离子键 | |
| B. | 元素Z的某种氧化物具有漂白性,是因为这种氧化物具有强氧化性 | |
| C. | 由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 | |
| D. | 元素W和M的某些单质可作为水处理中的消毒剂 |
20.化学中将具有的原子数相同、最外层电子数之和相同的粒子称为等电子体.下列各组中的物质属于等电子体的是( )
| A. | CN-和N2 | B. | NO和O2 | C. | NO2和CO2 | D. | SO2和ClO2 |
19.若阿伏加德罗常数的值为NA,则下列说法中正确的是( )
0 155964 155972 155978 155982 155988 155990 155994 156000 156002 156008 156014 156018 156020 156024 156030 156032 156038 156042 156044 156048 156050 156054 156056 156058 156059 156060 156062 156063 156064 156066 156068 156072 156074 156078 156080 156084 156090 156092 156098 156102 156104 156108 156114 156120 156122 156128 156132 156134 156140 156144 156150 156158 203614
| A. | 标准状况下,11.2 L SO3所含的分子数目为0.5NA | |
| B. | 1 molFe与过量的氯气反应,转移电子的数目为2 NA | |
| C. | 常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA | |
| D. | 50mL18.4mol•L-1的浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
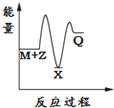
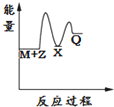
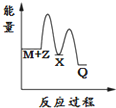
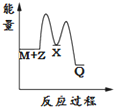
 Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料.
Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料.