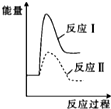
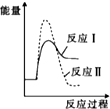
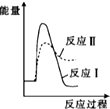
6.以下有关元素性质的说法不正确的是( )
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,原子半径最大的是① | |
| B. | 下列原子的外围电子排布中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,对应的第一电离能最大的是④ | |
| C. | ①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数的增加而递增的是④ | |
| D. | 某元素X的逐级电离能(kJ/mol)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时最可能生成的阳离子是X2+ |
5.下列关于价电子构型为4s24p4的基态原子描述正确的是( )
| A. | 它的元素名称为锡 | B. | 它的核外电子排布式为[Ar]4s24p4 | ||
| C. | 它的第一电离能小于As | D. | 其外围电子排布图为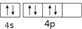 |
4.氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料.
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O;正极分压式为O2+4e-+2H2O=4OH-.
(2)下列措施可以加快合成氨反应速率的是ACDE.
A.通过缩小容器的容积增大压强
B.及时将氨液化分离出去
C.适当升温
D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
则从反应开始到25min时,①以N2表示的平均反应速率为0.01mol/(L.min);②H2的平衡转化率为50%;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(g);△H=+116kJ•mol-1
③H2O(l)═H2O(g);△H=+44kJ•mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式CO2(g)+2NH3(g)=CO(NH2)2(S)+H2O(1)△H=-87.47kJ/mol.
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O;正极分压式为O2+4e-+2H2O=4OH-.
(2)下列措施可以加快合成氨反应速率的是ACDE.
A.通过缩小容器的容积增大压强
B.及时将氨液化分离出去
C.适当升温
D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(g);△H=+116kJ•mol-1
③H2O(l)═H2O(g);△H=+44kJ•mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式CO2(g)+2NH3(g)=CO(NH2)2(S)+H2O(1)△H=-87.47kJ/mol.
2.绿色电源“二甲醚【(CH3)2O】-氧气燃料电池”的工作原理如图所示,下列说法正确的是( )
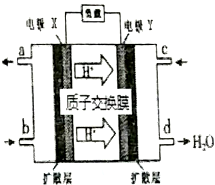

| A. | 氧气应从c处通入,电极Y上发生的反应为:O2+4e-+2H2O═4OH- | |
| B. | 电池在放电过程中,电极X周围溶液的pH增大 | |
| C. | 当该电池向外电路提供2 mol电子时消耗O2约为11.2L | |
| D. | 二甲醚应从b处加入,电极X上发生的反应为:(CH3)2O-12e-+3H2O═2CO2+12H+ |
1.当浓度恒定时,A、B两种物质在不同温度下进行反应:A+3B?3C.10℃时,反应率v(B)=0.3mol/(L•s);50℃时,反应速率v(A)=25.6mol/(L•s).若该反应温度升高10℃反应速率增至原来的n倍,则n值为( )
| A. | 4 | B. | 3 | C. | 3.5 | D. | 2.5 |
19.如图是部分短周期元素原子序数与最外层电子数之间的关系图,下列说法中正确的是( )


| A. | 元素对应的离子半径:Z>M>R>W | |
| B. | 简单氢化物的沸点:W>R>Y>X | |
| C. | 气态氢化物的稳定性:X>Y>R>W | |
| D. | Z、X、R、W的最高价氧化物对应的水化物均能与N的单质反应 |
17.下列化学用语书写正确的是( )
0 155958 155966 155972 155976 155982 155984 155988 155994 155996 156002 156008 156012 156014 156018 156024 156026 156032 156036 156038 156042 156044 156048 156050 156052 156053 156054 156056 156057 156058 156060 156062 156066 156068 156072 156074 156078 156084 156086 156092 156096 156098 156102 156108 156114 156116 156122 156126 156128 156134 156138 156144 156152 203614
| A. | 作为相对原子质量标准的原子${\;}_{6}^{14}$C | |
| B. | 氯化镁的电子式: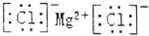 | |
| C. | 用电子式表示氯化氢分子的形成过程: | |
| D. | HClO的结构式为:H-Cl-O |
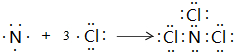 ;
;